
科目: 来源: 题型:
【题目】用软锰矿(主要成分为MnO2,含少量Fe3O4、Al2O3)和BaS制备高纯MnCO3的工艺流程如下:
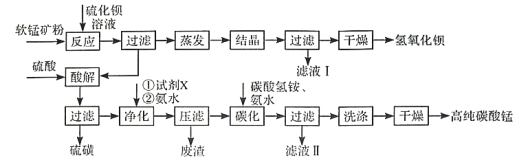
已知:MnO2是一种两性氧化物;25℃时相关物质的Ksp见下表。
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
Ksp |
|
|
|
|
回答下列问题
(1)软锰矿预先粉碎的目的是____________,MnO2与BaS溶液反应转化为MnO的化学方程式为________。
(2)保持BaS投料量不变,随MnO2与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是________。
(3)滤液I可循环使用,应当将其导入到________操作中(填操作单元的名称)。
(4)净化时需先加入的试剂X为________(填化学式)。再使用氨水调溶液的pH,则pH的理论最小值为_______(当溶液中某离子浓度![]() 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(5)碳化过程中发生反应的离子方程式为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 溶液与
溶液与![]() 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为![]() ,反应后最高温度为
,反应后最高温度为![]() 。
。
已知:反应前后,溶液的比热容均近似为![]() 、溶液的密度均近似为
、溶液的密度均近似为![]() ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量![]() _____J。
_____J。
(2)反应![]() 的
的![]() ______
______![]() (列式计算)。
(列式计算)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知(b)![]() 、(d)
、(d)![]() 、(p)
、(p)![]() 的分子式均为C6H6,下列说法正确的是
的分子式均为C6H6,下列说法正确的是
A. b的同分异构体只有d和p两种B. b、d、p的二氯代物均只有三种
C. b、d、p均可与酸性高锰酸钾溶液反应D. b、d、p中只有b的所有原子处于同一平面
查看答案和解析>>
科目: 来源: 题型:
【题目】现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL、0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有__________(填代号)。
(2)经计算,需浓H2SO4的体积为____________。现有①10 mL ②50 mL ③100 mL三种规格的量筒,你选用的量筒是__________(填代号)。
(3)将浓H2SO4加适量蒸馏水稀释后,冷却片刻,随后全部转移到__________ mL的容量瓶中,转移时应用玻璃棒__________。转移完毕,用少量蒸馏水洗涤__________2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度__________处。改用__________加蒸馏水到瓶颈刻度的地方,使溶液的__________。振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,下列操作中:错误的是_______,能引起误差偏高的有______(填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A.1mol的羟基与1mol的氢氧根离子所含电子数均为9NA
B.常温常压下,18g H2O含有的原子总数为3NA
C.标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA
D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】白藜芦醇广泛存在于食物(例如桑甚、花生,尤其是葡萄)中,它可能具有抗癌性。能够与1 mol该化合物发生反应的Br2和H2的最大用量分别是( )

A.1mol、1molB.3.5mol、7mol
C.3.5mol、6molD.6mol、7mol
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.32![]() 中含有的氧原子数是2×6.02×1023
中含有的氧原子数是2×6.02×1023
B.N2和CO共1mol的混合气体中含有的分子总数是2×6.02×1023
C.2.3 g Na与O2完全反应生成3.6 g产物时失电子数是0.1×6.02×1023
D.1.0 L 0.1 mol·L-1NH4NO3溶液中含有的铵根离子数是0.1×6.02×1023
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠在纺织业等领域有广泛应用。某兴趣小组用下图装置制备![]() 。
。

合成反应:![]()
![]()
![]()
滴定反应:![]()
已知:![]() 易溶于水,难溶于乙醇,
易溶于水,难溶于乙醇,![]() 开始失结晶水。
开始失结晶水。
实验步骤:
Ⅰ.![]() 制备:装置A制备的
制备:装置A制备的![]() 经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液
经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液![]() 约为7时,停止通入
约为7时,停止通入![]() 气体,得产品混合溶液。
气体,得产品混合溶液。
Ⅱ.产品分离提纯:产品混合溶液经蒸发浓缩、冷却结晶、过滤洗涤、干燥,得到![]() 产品。
产品。
Ⅲ.产品纯度测定:以淀粉作指示剂,用![]() 产品配制的溶液滴定碘标准溶液至滴定终点,计算
产品配制的溶液滴定碘标准溶液至滴定终点,计算![]() 含量。
含量。
请回答:
(1)步骤Ⅰ:单向阀的作用是______;装置C中的反应混合溶液![]() 过高或过低将导致产率降低,原因是_______。
过高或过低将导致产率降低,原因是_______。
(2)步骤Ⅱ:下列说法正确的是_____。
A 快速蒸发溶液中水分,可得较大晶体颗粒
B 蒸发浓缩至溶液表面出现品晶膜时,停止加热
C 冷却结晶后的固液混合物中加入乙醇可提高产率
D 可选用冷的![]() 溶液作洗涤剂
溶液作洗涤剂
(3)步骤Ⅲ
①滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):
检漏→蒸馏水洗涤→(______)→(______)→(______)→(______)→(______)→开始滴定。
A 烘干 B 装入滴定液至零刻度以上 C 调整滴定液液面至零刻度或零刻度以下D 用洗耳球吹出润洗液 E 排除气泡 F 用滴定液润洗2至3次 G 记录起始读数
②装标准碘溶液的碘量瓶(带瓶塞的锥形瓶)在滴定前应盖上瓶塞,目的是______。
③滴定法测得产品中![]() 含量为
含量为![]() ,则
,则![]() 产品中可能混有的物质是________。
产品中可能混有的物质是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com