
科目: 来源: 题型:
【题目】在甲、乙、丙、丁四个烧杯中分别放入![]() 的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
A.甲<乙<丙<丁B.丁<甲<乙=丙C.甲=丁<乙=丙D.丁<甲<乙<丙
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室有NaHSO4、Ba(OH)2、NH3·H2O、NaHCO3、KAl(SO4)2五种无色溶液,现欲通过它们之间的相互反应的现象对其进行鉴别。部分物质间的反应现象如表。
A | B | C | D | E | |
A | ↓ | ||||
B | ↑ | ↓ | |||
C | ↑ | ↑↓ | ↓ | ||
D | ↓ | ↑↓ | ↓ | ||
E | ↓ | ↓ | ↓ |
表中“↑”表示生成气体物质,“↓”表示生成沉淀。根据以上信息,回答以下问题。
(1)B,E的化学式分别为________、________。
(2)写出A的电离方程式:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关叙述正确的是( )
A.由反应:M(s)+N(g) ![]() R(g) △H1 ,M(g)+N(g)
R(g) △H1 ,M(g)+N(g) ![]() R(g) △H2,得出△H 2>△H 1
R(g) △H2,得出△H 2>△H 1
B.已知:2SO2(g)+O2(g) ![]() 2SO3(g);△H=-98.3kJ/mol。将1molSO2和0.5molO2充入一密闭容器中反应,放出49.15kJ的热量
2SO3(g);△H=-98.3kJ/mol。将1molSO2和0.5molO2充入一密闭容器中反应,放出49.15kJ的热量
C.电解精炼铜时,电源负极与纯铜相连,且电解质溶液浓度始终保持不变
D.用惰性电极电解 Na2SO4溶液,当阴极产生1mol气体时,可加18 g 水使溶液恢复
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验操作能达到实验目的的是( )

A.用pH试纸测量氯水的pH
B.将4.0 g NaOH固体置于100 mL容量瓶中,加水至刻度, 配制1.000 mol·L1NaOH溶液
C.用装置甲蒸发浓缩MgCl2溶液,再冷却结晶制MgCl2·6H2O固体
D.用装置乙除去氯气中的少量HCl杂质
查看答案和解析>>
科目: 来源: 题型:
【题目】最近我国科学家预测并据此合成了新型碳材料:T-碳。可以看作金刚石结构中的一个 碳原子被四个碳原子构成一个正四面体结构单元替代(如图所示,所有小球都代表碳原子)。下列说法正确的是( )
金刚石 T-碳
T-碳
A.T-碳与石墨、金刚石互为同分异构体
B.T-碳晶体与金刚石晶体类似,属于原子晶体
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子采取的杂化方式不同
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家通过测量SiO2中26 Al和10 Be两种元素的比例来确定“北京人”的年龄,这种测量方法叫铝铍测年法。下列关于26 Al和10 Be的说法不正确的是( )
A.5.2g 26 Al3+中所含的电子数约为1.204×1024
B.10 Be和9 Be是中子数不同、质子数相同的不同原子
C.26 Al3+和26 Mg2+的质子数、中子数和核外电子数都不相同
D.10 Be原子核内的中子数比质子数多
查看答案和解析>>
科目: 来源: 题型:
【题目】从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如下:
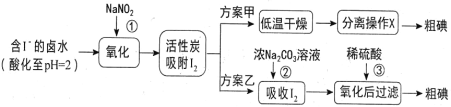
资料显示:
Ⅰ.pH=2 时, NaNO2 溶液只能将 I-氧化为 I2,同时生成 NO;
Ⅱ.I2+5Cl2+6H2O=2HIO3+10HCl;
Ⅲ.I2在碱性溶液中反应生成I-和IO3-。
(1)反应①的离子方程式_____。
(2)方案甲中,根据 I2的特性,分离操作 X 的名称是_____。
(3)Cl2、酸性 KMnO4 等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO2,原因是_____。
(4)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I2、I-、IO3-。 请检验滤液中的I-,将实验方案补充完整。实验中可供选择的试剂:稀 H2SO4、淀粉溶液、Fe2(SO4)3 溶液。
A.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
B._____。
查看答案和解析>>
科目: 来源: 题型:
【题目】“生活无处不化学”,回答下列问题:
(1)用白醋浸泡开水壶,第二天发现壶内水垢消失,开水壶又光洁如新了(水垢的主要成分是碳酸钙等)。该离子反应方程式为____________。
(2)食盐不慎洒落在天然气的火焰上,观察到的现象是_____,该变化称为_____反应。
(3)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是____________。
(4)面包在制作时会加入小苏打,利用其加热产生气体的性质,可将小苏打作为膨松剂,该反应的化学方程式是________________。
(5)光导纤维、沙子、石英和玛瑙的主要成分是__________(填化学式)。
(6)赏心悦目的雕花玻璃是用__________(填名称)对玻璃进行刻蚀而制成的。
(7)使用“84”消毒液(含NaClO)时,按一定比例将它与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,以达到杀菌消毒的效果更好的目的。将该反应的离子方程式补充完整:![]() ____+____。
____+____。
查看答案和解析>>
科目: 来源: 题型:
【题目】ZrO2是重要的耐温材料,可用作陶瓷遮光剂。天然锆英石(ZrSiO4)含有铁、铝、铜等金属元素的氧化物杂质,工业以锆英石为原料制备ZrO2的工艺流程如下:
已知:①锆英石中锆元素的化合价为+4 ,“氯化”过程中除C、O元素外,其他元素均转化为最高价氯化物 ②SiCl4极易水解;ZrCl4易溶于水 ③Fe(SCN)3难溶于有机溶剂MIBK; Zr(SCN)4在水中溶解度不大,易溶于有机溶剂MIBK。
(1) “氯化”过程中,锆英石发生的主要反应的化学方程式为:______________________________,ZrC14的产率随温度变化如图所示,由图可知氯化的最佳条件是_____________;

(2)“滤液1”中含有的阴离子除OH- 、Cl-,还有___________________;
(3)常用的铜抑制剂有Na2S、H2S、NaCN等,本流程使用NaCN除铜,不采用Na2S、H2S的原因是__________。
(4)实验室进行萃取和反萃取的玻璃仪器是_______。流程中萃取与反萃取的目的是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】把7.5 g镁铝合金的粉末放入200ml 4mol/L的盐酸中,往充分反应后的混合溶液中逐渐滴入一定物质的量浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如图所示。

(1)合金中镁的物质的量为_______。
(2)氢氧化钠的物质的量浓度为_______mol/L。
(3)V1=_______mL。
(4)写出该合金溶于足量NaOH溶液的化学方程式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com