
科目: 来源: 题型:
【题目】请完成下列问题:
(1)Cl2和水蒸气通过灼热的炭层生成HCl和CO2,当有1 mol Cl2参与反应时释放145 kJ热量。写出该反应的热化学方程式____________________________。
(2)已知CH3OH(l)的燃烧热为238.6 kJ·mol-1,CH3OH(l)+1/2O2(g) =CO2(g)+2H2O(g) ΔH=-a kJ·mol-1,则a_______238.6(选填“>”、“<”或“=”)。
(3)已知:As(s)+3/2H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+1/2O2(g)=H2O(l) ΔH2
2As(s)+5/2O2(g) =As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)已知在一定温度下:
C(s)+ CO2(g)![]() 2CO(g) 平衡常数K1
2CO(g) 平衡常数K1
C(s)+ H2O(g)![]() CO(g)+ H2(g) 平衡常数 K2
CO(g)+ H2(g) 平衡常数 K2
CO(g)+ H2O(g)![]() H2(g)+ CO2(g)平衡常数K3
H2(g)+ CO2(g)平衡常数K3
则K1、K2、K3之间的关系是__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】消除含氮化合物对大气和水体的污染是环境保护的重要研究课题。
(1)已知反应8NH3+6NO2=7N2+12H2O,请分析氧化产物和还原产物的质量之比为________。
(2)水体中过量氨氮(以NH3表示)会导致水体富营养化。
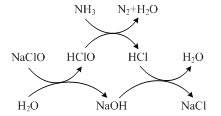
①用次氯酸钠除去氨氮的原理如题图所示。写出该图示的总反应化学方程式:________。
该反应需控制温度,温度过高时氨氮去除率降低的原因是________。
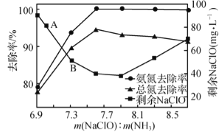
②取一定量的含氨氮废水,改变加入次氯酸钠用量,反应一段时间后,溶液中氨氮去除率、总氮(溶液中所有可溶性的含氮化合物中氮元素的总量)去除率以及剩余次氯酸钠的含量随m(NaCIO)m(NH3)的变化情况如图所示。当m( NaCIO):m(NH3)>7.6时,水体中总氮去除率反而下降,可能的原因是________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学(离子)方程式
(1)HF不能装在玻璃瓶中,对应发生的化学方程式________
(2)NO2与一定量的O2混合通入水中,完全被水吸收的离子方程式________
(3)Pb的常见化合价是+2价和+4价,PbO2的某些化学性质与MnO2相似。写出实验室用PbO2与浓盐酸混合加热制氯气的化学方程式________
(4)SO2气体使溴水褪色的离子方程式________
(5)煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323K,NaClO2溶液浓度为5×10-3mol·L-1.(溶液呈碱性)反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42- | SO32- | NO3- | NO2- | Cl= |
c/(mol·L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
写出NaClO2溶液脱硝过程中主要反应的离子方程式 ________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、M均为短周期元素,M的一种核素不含中子,X、Y、Z、W在周期表中的位置如图所示,Y原子最外层电子数为内层电子数的3倍。下列说法不正确的是
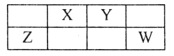
A. 原子半径:Z>X>Y>M
B. X、Y、Z、W与M均能形成18电子分子
C. X、Y、M形成的化合物水溶液一定呈酸性
D. Y的简单阴离子还原性弱于X的简单阴离子还原性
查看答案和解析>>
科目: 来源: 题型:
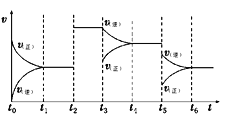
【题目】某密闭容器中发生反应:2A(g)+B(g)![]() 2C(g) ΔH ,图1表示该反应在不同温度下B的转化率随温度变化曲线,图2表示该反应的反应速率(v)随时间(t)变化图像。
2C(g) ΔH ,图1表示该反应在不同温度下B的转化率随温度变化曲线,图2表示该反应的反应速率(v)随时间(t)变化图像。

请回答下列问题:
(1)图中a、b、c三点的化学反应速率(v)由快到慢是__________。
(2)图中该反应的ΔH_______0。
(3)图中a、b、c三点,未达到平衡状态且v正>v逆的点是_______。
请回答下列问题:
(4)图中t2时刻改变的外界条件是___________。
(5)图中从t1 ~ t6 反应物转化率最低的是_______时刻。
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应:2A(s) ![]() B(g)+C(g),在一定条件下的刚性密闭容器中,起始时加入一定量的A,能判断反应达到平衡状态的有( )
B(g)+C(g),在一定条件下的刚性密闭容器中,起始时加入一定量的A,能判断反应达到平衡状态的有( )
①单位时间内生成2molA的同时生成1molB ②v (B): v (C)=1:1 ③密闭容器中混合气体的平均摩尔质量不变 ④混合气体的密度不再改变 ⑤B的体积分数不再改变 ⑥混合气体的压强不再改变
A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究矿物固体X(仅含4种短周期元素)的组成和性质,其中固体乙可制作光导纤维。现完成如下实验:
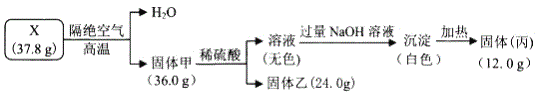
请回答:
(1)X的化学式为_____。
(2)X中所含的一种金属元素是___填元素符号),其单质在![]() 中燃烧的化学方程式为_____。
中燃烧的化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】用于净化汽车尾气的反应:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g),已知该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
2CO2(g)+N2(g),已知该反应速率极慢,570K时平衡常数为1×1059。下列说法正确的是
A.装有尾气净化装置的汽车排出的气体中一定不再含有NO或CO
B.提高尾气净化效率的常用方法是升高温度
C.提高尾气净化效率的最佳途径是研制高效催化剂
D.570K时该反应正向进行的程度很大,故使用催化剂并无实际意义
查看答案和解析>>
科目: 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:

下列说法不正确的是( )
A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为21
B.反应①氧化产物与还原产物的物质的量之比为1:1
C.反应②条件下,ClO2的氧化性大于H2O2反应
D.②中的H2O2可用NaClO4代替
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com