
科目: 来源: 题型:
【题目】R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应,X2++Z=X+Z2+,Y+Z2+=Y2++Z。这四种离子被还原成0价时,表现的氧化性强弱顺序为( )
A.R2+>X2+>Z2+>Y2+B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+D.Z2+>X2+>R2+>Y2+
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,盐酸与氢氧化钠溶液相互滴定的滴定曲线如下图,下列叙述不正确的是
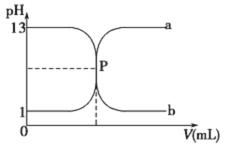
A. 滴定过程的任何时刻都存在:c(H+)+ c(Na+)=c(OH-)+c(Cl-)
B. 曲线b是用氢氧化钠溶液滴定盐酸溶液的滴定曲线
C. 氢氧化钠溶液的物质的量浓度为0.1molL-1
D. P点时恰好完全中和,溶液呈中性
查看答案和解析>>
科目: 来源: 题型:
【题目】化学土肥外加少量酸、碱,而pH基本不变的溶液,称为缓冲溶液,现有25℃时,浓度均为0.10mol/L的CH3COOH和CH3COONa的缓冲溶液,pH=4.76,回答下列问题:
[Ka(CH3COOH)=1.75×10-5,Kb为盐的水解常数]
(1)CH3COOH的电离方程式为__。
(2)该缓冲溶液中离子浓度由大到小的顺序是___。
(3)25℃时,Ka(CH3COOH)___Kb(CH3COO-)(填“>”“<”或“=”)。
(4)用1.0L上述缓冲溶液中滴加几滴NaOH稀溶液(忽略溶液体积的变化),反应后溶液中c(H+)__mol/L。
(5)人体血液存在H2CO3(CO2)与NaHCO3的缓冲体系,能有效除掉人体正常代谢产生的酸、碱,保持pH的稳定,有关机理说法正确的是__(填写选项字母)。
a.代谢产生的![]() 被HCO3-结合形成H2CO3
被HCO3-结合形成H2CO3
b.血液中的缓冲体系可抵抗大量酸、碱的影响
c.代谢产生的碱被H+中和,H+又由H2CO3电离补充
查看答案和解析>>
科目: 来源: 题型:
【题目】有7种短周期元素的原子序数按A、B、C、D、E、F、G 的顺序依次增大,B元素一种原子的含量常用于判定古生物遗体的年代,A和C元素的原子能形成4核10电子的微粒,D和E可形成离子化合物E2D,E2D中所有微粒的电子数相同,且电子总数为30,E、F、G的最高价氧化物对应的水化物之间可以相互反应,G和D同主族。试回答下列问题:
(1)C元素的原子结构示意图____________。
(2)A和D可形成化合物的化学式为__________________。
(3)F的单质与E元素的最高价氧化物对应的水化物反应的离子方程式为___________。
(4)上述元素形成的二元化合物中,能够用于漂白的气体物质中含有的化学键类型为___________。
(5)写出D 元素原子形成的10电子微粒X与G元素原子形成的18电子微粒Y反应的离子方程式:_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y是同周期的两种主族元素,他们的逐级电离能(I)数据如下表所示:
电离能(kJ/mol) | I1 | I2 | I3 | I4 | I5 | …… |
X | 496 | 4562 | 6912 | 9543 | 13353 | …… |
Y | 738 | 1451 | 7733 | 10540 | 13630 | …… |
下到有关说法正确的是( )
A.电负性:X<YB.与水反应剧烈程度:X<Y
C.X的最外层电子数为1D.Y的最高化合价为+3
查看答案和解析>>
科目: 来源: 题型:
【题目】关于一定条件下的化学平衡H2(g)+I2(g)![]() 2HI(g) ΔH<0,下列说法正确的是( )
2HI(g) ΔH<0,下列说法正确的是( )
A.恒温恒容,充入H2,v(正)增大,平衡右移
B.恒温恒容,充入He,v(正)增大,平衡右移
C.加压,v(正),v(逆)不变,平衡不移动
D.升温,v(正)减小,v(逆)增大,平衡左移
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各反应中,氧化反应与还原反应在同种元素中进行的是
A.Cl2+2NaOH===NaCl+NaClO+H2O
B.2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
C.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】锌空气电池的电容量大,可作为汽车的清洁能源。总反应式为:2Zn+O2+2H2O=2Zn(OH)2。示意图如图所示:

有关该电池的说法正确的是( )
A.电池可以用稀硫酸做电解质溶液
B.电池工作时,电子由a电极沿导线流向b电极
C.空气扩散电极上的电极反应:O2+2H2O+4e-=4OH-
D.阻隔空气进入锌--空气电池,电池停止工作
查看答案和解析>>
科目: 来源: 题型:
【题目】已知2H2(g)+O2(g)=2H2O(l) ΔH1=-572kJ/mol
C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ/mol
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3=-1367kJ/mol
则2C(s)+3H2(g)+![]() O2(g)=C2H5OH(l),ΔH为( )
O2(g)=C2H5OH(l),ΔH为( )
A.+278kJ/molB.-278kJ/molC.+401.5kJ/molD.-401.5kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】化学家在氨的合成及利用氨制硝酸等方面做出了突出贡献。回答下列问题:
(1)N2和H2合成氨的化学方程式为___;为了降低能耗并提高原料利用率,科学家利用电解原理(两极间可传输![]() ),探索用N2和H2制备NH3,预测阴极的反应式为___。
),探索用N2和H2制备NH3,预测阴极的反应式为___。
(2)制备硝酸主要有三步转化过程:

反应I的转化利用了NH3的__性,每生成1molNO转移电子数为___NA。
反应Ⅲ:3NO2(g)+H2O(l)![]() 2HNO3(aq)+NO(g) ΔH<0,下列措施不能提高NO2吸收率的是__(填写选项字母)。
2HNO3(aq)+NO(g) ΔH<0,下列措施不能提高NO2吸收率的是__(填写选项字母)。
a.增大压强 b.降低温度 c.使用催化剂
(3)硝酸工业的尾气成分主要是NOx,通常利用NH3处理,将其转化为无毒物质后排放,该反应的化学方程式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com