
科目: 来源: 题型:
【题目】海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法正确的是
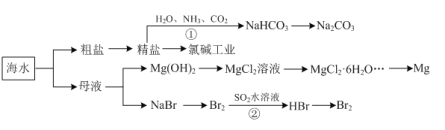
A.由反应①可知:相同温度下,NaHCO3的溶解度大于Na2CO3
B.MgCl2溶液通过蒸发浓缩、冷却结晶可获得MgCl2·6H2O
C.反应②的离子方程式为:Br2+SO2+2H2O=SO42—+2Br—+4H+
D.粗盐中含有的Mg2+、SO42—等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等试剂加以去除
查看答案和解析>>
科目: 来源: 题型:
【题目】软质隐形眼镜材料W、树脂X的合成路线如图所示。
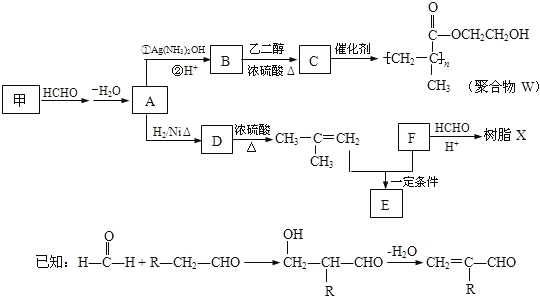
(1)A 中含有的官能团名称是_________。
(2)甲的结构简式是_____________。
(3)B→C反应的化学方程式是______________________________________________。
(4)B有多种同分异构体.属于酯且含有碳碳双键的同分异构体共有______种(不考虑顺反异构,下同),写出其中能发生银镜反应,且含有甲基的所有同分异构体的结构简式是___________。
(5)已知F的相对分子质量为110,分子中碳原子、氢原子数都是氧原子数的3倍,苯环上的氢原子化学环境都相同.则F还能发生的反应是________(填序号)。
A.加成反应 b.氧化反应 c.加聚反应 D.水解反应
(6)写出树脂X可能的结构简式___________(写出一种即可)。
(7)E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种,生成E的化学方程式是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】海水中溴含量约为65mg·L-1,从海水中提取溴的工艺流程如下:
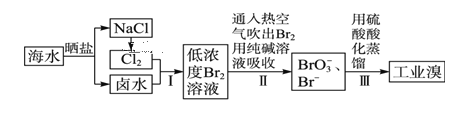
(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是_______。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的__________。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在下面横线上填入适当的化学计量数:_____Br2+_____CO32-=_____ BrO3-+_____Br-+_____CO2↑
(4)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的化学方程式:__________。
(5)实验室分离溴还可以用溶剂萃取法,下列可以用作溴的萃取剂的是__________。
A.乙醇 B.四氯化碳 C.烧碱溶液 D.苯
查看答案和解析>>
科目: 来源: 题型:
【题目】向1 L FeCl3与CuCl2的混合溶液(其中Cu2+浓度为0.05 mol·L-1)中加入一定量的Fe粉,充分反应后过滤,剩余固体质量为6.0 g,向滤液中加入足量的AgNO3溶液,生成57.4 g沉淀。下列说法正确的是
A.剩余固体为CuB.加入Fe粉的质量为8.4 g
C.原溶液中Fe3+浓度为0.3 mol·L-1D.反应后溶液中Fe2+浓度为0.2 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B均是由一种金属元素和一种非金属元素组成的化合物,A中金属元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为常见的无色液体。反应生成的水均已略去。它们有如图所示的关系。

(1)写出B的化学式:___;
(2)反应③中每生成1molF,转移电子的数目为___;
(3)反应④的化学方程式为:___;
(4)写出少量H与G发生反应②的离子方程式:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】㈠下列有关实验的叙述,正确的是(填序号)______________
A、用NaOH溶液除去乙酸乙酯中混有的乙酸、乙醇,然后分液
B、分馏石油时,温度计的末端必须插入液面下
C、用分液漏斗分离环己烷和水的混合液体
D、用浓氨水洗涤做过银镜反应的试管
E、配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止
F、蔗糖水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖
㈡某化学活动小组设计以下装置进行不同的实验。其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c中盛有冰水。

(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是____(填序号),该装置中应加入试剂__________。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入的固体物质是__________。
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是_________(填序号),再用制得的乙醛溶液进行银镜反应,正确的操作顺序是_____________。
A、②④①③ B、④②③① C、④②①③ D、④①②③
①向试管中滴入3滴乙醛溶液。②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止。③振荡后放入热水中,水浴加热。④在洁净的试管中加入1mL2%的AgNO3溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色混合溶液中可能含有的离子如下表所示:
可能大量含有的阳离子 | H+、Al3+、NH4+、Na+ |
可能大量含有的阴离子 | Cl-、AlO2-、SO42-、MnO4-、Br-、I-、CO32- |
为探究其成分,进行了以下探究实验。
探究一:
甲同学取一定量的混合溶液,用pH试纸检验,溶液pH<7;向其中逐液加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示。
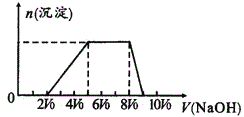
探究二
乙同学取一定量的混合溶液,向溶液中加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
探究三:
另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
(1)该溶液中一定含有的阴离子是___;其中能确定离子浓度之比的,对应离子物质的量浓度之比为___;不能肯定是否含有的离子是___。确定其中阳离子的实验方法为___。
(2)请写出沉淀减少过程中发生反应的离子方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚砜(SOCl2)常用于医药、农药、染料工业,也可在有机合成工业中作氯化剂。已知:SOCl2的相关性质如下表所示:
颜色、状态 | 熔点 | 沸点 | 腐蚀性 | 水解 |
无色或微黄液体 | -105℃ | 78℃ | 强 | 极易水解 |
现利用如图装置制备SOCl2。
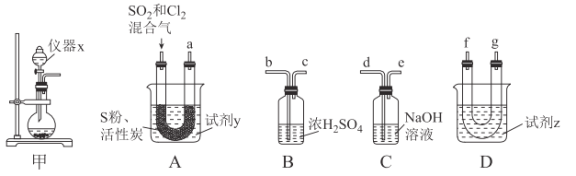
请回答下列问题:
Ⅰ.制备SO2和Cl2。
(1)本实验选用装置甲制备SO2和Cl2,装置甲中仪器x的名称为___;若以KMnO4和浓盐酸反应制备Cl2,反应的离子方程式为___。
Ⅱ.制备SOCl2。
以活性炭作为催化剂,SO2和C12可以和S粉在180~200℃时反应合成SOCl2,选用装置A、B、C、D进行制备(夹持、加热装置略去)。
(2)按气流从左到右的方向,装置A、B、C、D的连接顺序为___(填仪器接口的字母编号)。
(3)试剂y为___(填选项字母,下同);试剂z为___。
A.热水 B.乙醇 C.石蜡油 D.冰水
(4)装置A中U形管内发生反应的化学方程式为___。
(5)装置C的作用为___;若装置A处通入的SO2和Cl2的物质的量之比为1:3,则装置C中生成的盐为___(填化学式);请设计实验验证装置C中生成的盐中含有SO42-:____。
查看答案和解析>>
科目: 来源: 题型:
【题目】酯化反应是酸与醇发生反应生成酯和水的反应。下列反应属于酯化反应的是( )
A.CH3COOH+NaOH→CH3COONa+H2O
B.CH2==CHCOOCH3+H2![]() CH3CH2COOCH3
CH3CH2COOCH3
C.CH3COOCH2CH3+H2O![]() CH3COOH+CH3CH2OH
CH3COOH+CH3CH2OH
D.2CH3COOH+HOCH2CH2OH![]() CH3COOCH2CH2OOCCH3+2H2O
CH3COOCH2CH2OOCCH3+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】已知酸性高锰酸钾溶液可以将FeSO4氧化,化学方程式为2KMnO4+10FeSO4+8H2SO4===K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示。则下列有关说法不正确的是( )
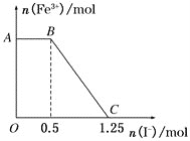
A. 图中AB段主要是高锰酸钾和碘化钾溶液反应
B. 图中BC段发生的反应为2Fe3++2I-===2Fe2++I2
C. 根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol
D. 根据OC段的数据可知开始加入的硫酸亚铁的物质的量为1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com