
科目: 来源: 题型:
【题目】已知![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 是原子序数依次增大的短周期主族元素,
是原子序数依次增大的短周期主族元素,![]() 核内只有1个质子,
核内只有1个质子,![]() 原子最外层电子数是次外层电子数的3倍,
原子最外层电子数是次外层电子数的3倍,![]() 的二价阳离子与氖原子具有相同的核外电子排布,
的二价阳离子与氖原子具有相同的核外电子排布,![]() 与
与![]() 同主族,下列说法正确的是( )
同主族,下列说法正确的是( )
A.![]() 的原子半径在五种原子中最大
的原子半径在五种原子中最大
B.一定条件下,![]() 的单质能与水反应
的单质能与水反应
C.![]() 与
与![]() 形成的化合物只有一种
形成的化合物只有一种
D.![]() 的最高价氧化物的水化物的酸性比
的最高价氧化物的水化物的酸性比![]() 的弱
的弱
查看答案和解析>>
科目: 来源: 题型:
【题目】已知同周期的![]() 、
、![]() 、
、![]() 三种元素的最高价氧化物的水化物的酸性由强到弱的顺序为
三种元素的最高价氧化物的水化物的酸性由强到弱的顺序为![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.三种元素的原子序数按![]() 、
、![]() 、
、![]() 的顺序增大
的顺序增大
B.单质的氧化性按![]() 、
、![]() 、
、![]() 的顺序减弱
的顺序减弱
C.原子半径按![]() 、
、![]() 、
、![]() 的顺序增大
的顺序增大
D.气态氢化物的稳定性按![]() 、
、![]() 、
、![]() 的顺序增强
的顺序增强
查看答案和解析>>
科目: 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是
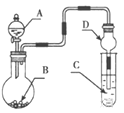
A.若A为H2O2,B为MnO2,C中盛有Na2S溶液, C中溶液变浑浊
B.若A为浓盐酸,B为MnO2,C中盛有KI淀粉溶液,C中溶液变蓝色
C.若A为浓氨水,B为生石灰,C中盛有AlCl 3溶液, C中先产生白色沉淀后沉淀又溶解
D.若A为浓H2SO4 ,B为CaCO3,C中盛有Na2SiO3 溶液,C中溶液出现白色沉淀,证明非金属性S>C>Si
查看答案和解析>>
科目: 来源: 题型:
【题目】将红热的固体单质M放入浓硝酸中,剧烈反应,产生混合气体A,A在常温下不与空气接触时,发生如图所示的变化。
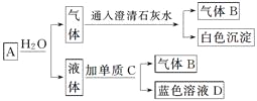
(1)混合气体A的主要成分是____________。
(2)气体B为__________,蓝色溶液D为____________。
(3)单质M与浓硝酸反应的化学方程式是____________________________。
(4)单质C与稀硝酸反应的化学方程式是________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.测定化学反应速率
某同学利用如图装置测定化学反应速率。
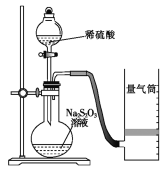
(已知:S2O32-+2H+=H2O+S↓+SO2↑)
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是__;除如图所示的实验用品、仪器外,还需要的一件实验仪器是__。
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是___。
Ⅱ.为探讨化学反应速率的影响因素
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。已知:5H2C2O4+2KMnO4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
实验时,通过测定褪色所需时间来判断反应的快慢。限选试剂与仪器:0.20mol/LH2C2O4溶液,0.010mol/L酸性KMnO4溶液,蒸馏水,锥形瓶,恒温水浴槽,量筒,秒表。该小组设计了如下的方案。
物理量 | 水 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
体积/mL | 浓度/molL-1 | 体积/mL | 浓度/molL-1 | 体积/mL | ||
① | 0 | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
② | 0 | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 1.0 | 0.010 | 4.0 | 25 | ||
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为:n(H2C2O4):n(KMnO4)≥__。
(2)实验③测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=__mol·L-1·min-1。
(3)请完成表格内二处空白__、__。
(4)已知50℃时c(MnO4-)~反应时间t的变化曲线如图。其中反应速率最快的阶段是__,原因是___。

查看答案和解析>>
科目: 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:
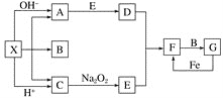
(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目: 来源: 题型:
【题目】四种位于不同主族的短周期元素X、Y、Z、W的原子序数依次增大,![]() 的内层电子与最外层电子数之比为2:5,Z和W位于同一周期。Z与W组成的化合物是常用的调味品,也是重要的医用药剂,工业上电解该化合物的熔融物可制得Z单质,Y和Z可形成两种离子化合物,这两种离子化合物的阴离子与阳离子数之比均为1:2。下列说法正确的是
的内层电子与最外层电子数之比为2:5,Z和W位于同一周期。Z与W组成的化合物是常用的调味品,也是重要的医用药剂,工业上电解该化合物的熔融物可制得Z单质,Y和Z可形成两种离子化合物,这两种离子化合物的阴离子与阳离子数之比均为1:2。下列说法正确的是
A. 四种元素中至少有两种金属元素
B. 四种元素的常见氢化物中熔点最高的是![]() 的氢化物
的氢化物
C. 四种元素形成的简单高子中,离子半径最小的是元素![]() 形成的离子
形成的离子
D. 常温下,![]() 三种元素形成的化合物的水溶液的
三种元素形成的化合物的水溶液的![]() 小于7
小于7
查看答案和解析>>
科目: 来源: 题型:
【题目】工业废弃物的资源化回收再利用,可以更大限度的发挥原材料的价值。下图是工业生产纳米磁性氧化铁的流程:

下列说法不正确的是
A. 用Na2CO3溶液浸泡是为了除去废铁屑表面的铁锈
B. 若生产中不通入N2,暴露在空气中生产,将不能得到高纯度产品
C. 加适量的H2O2是为了将部分Fe2+氧化为Fe3+ ,涉及反应:H2O2+2Fe2++2H+=2Fe3++2H2O
D. 溶液A中Fe2+和Fe3+的浓度比为1:2
查看答案和解析>>
科目: 来源: 题型:
【题目】图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量。下列反应对应的曲线正确的是

A. A曲线表示向AlCl3溶液中滴入NaOH溶液至过量
B. B曲线表示向Na[Al(OH)4]溶液中滴入HNO3溶液至过量
C. C曲线表示向n(HCl):n(AlC13)=1:1的混合溶液中滴入NaOH溶液至过量
D. D曲线表示向n[Ca(OH)2]:n(KOH)=1:2的混合溶液中通入CO2至沉淀消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com