
科目: 来源: 题型:
【题目】朱自清先生在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾所形成的种种美景的本质原因是( )
A.光是一种胶体B.雾是一种胶体
C.发生丁达尔效应D.空气中的小水滴颗粒大小约为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组在容积固定为2 L的密闭容器内充入1 mol N2和3 mol H2合成NH3。恒温下开始反应,并用压力传感器测定压强如下表所示:
反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
下列说法不正确的是
A.不断地将NH3液化并移走,有利于反应正向进行
B.其它条件不变,在30 min时,若压缩容器的体积,N2的平衡转化率增大
C.从反应开始到10 min时,v(NH3)=0.035 mol·L1·min1
D.在30 min时,再加入0.5 mol N2、1.5 mol H2和2 mol NH3,平衡向逆反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】在常温下,向20 mL浓度均为0.1 mol·L1的盐酸和氯化铵混合溶液中滴加0.1 mol·L1的氢氧化钠溶液,溶液pH随氢氧化钠溶液加入体积的变化如图所示(忽略溶液体积变化)。下列说法正确的是
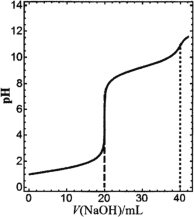
A.V(NaOH)=20 mL时,2n(![]() )+n(NH3·H2O)+n(H+)-n(OH)=0.1 mol
)+n(NH3·H2O)+n(H+)-n(OH)=0.1 mol
B.V(NaOH)=40 mL时,c(![]() )<c(OH)
)<c(OH)
C.当0<V(NaOH)<40 mL时,H2O的电离程度一直增大
D.若改用同浓度的氨水滴定原溶液,同样使溶液pH=7时所需氨水的体积比氢氧化钠溶液要小
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列物质:①Cl2 ②SO2 ③0.1mol·L-1Na2CO3溶液中的溶质 ④0.1mol·L-1的氨水中的NH3·H2O ⑤0.1mol·L-1CH3COOH溶液中的溶质 ⑥BaSO4。
(1)属于强电解质的是_____,属于弱电解质的是_____,属于非电解质的是_______,向⑤中加入等物质的量④,溶液导电性____(填“增强”或“减弱”)。
(2)已知③溶液呈碱性,甲同学认为显碱性原因是CO32-水解所致,为证明上述观点是否正确,请设计一个简单的实验,简述实验过程。___________。
(3)在T℃时,反应2SO2(g)+O2(g)![]() 2SO3(g) △H<0的平衡常数K=6×102,则:
2SO3(g) △H<0的平衡常数K=6×102,则:
①温度升高,化学平衡移动后,平衡常数K值________(填“增大”、“减少”或“不变”)。
②T℃时,向容积为2L的密闭容器中充入0.4molSO2、0.18molO2和1.2molSO3的混合气体,此时该反应是否处于化学平衡状态____(填“是”或“否”),化学反应速率v(正)___v(逆)(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨是一种重要的化工原料,可以用来制备氮化硅(Si3N4)肼(N2H4)、氢氰酸(HCN)。
(1)已知:Si(s)+2Cl2(g)====SiCl4(g) △H1=akJ·mol-1
N2(g)+3H2(g) ![]() 2NH3(g) △H2=bkJ·mol-1
2NH3(g) △H2=bkJ·mol-1
3Si(s)+2N2(g)====Si3N4(s) △H3=ckJ·mol-1
H2(g)+Cl2(g)====2HCl(g) △H4=dkJ·mol-1
则反应3SiCl4(g)+4NH3(g)====Si3N4(s)+12HCl(g)的△H=________________kJ·mol-1(用a、b、c、d表示)。
(2)肼的制备方法是用次氯酸钠氧化过量的氨。
已知ClO-水解的方程式为:ClO-+H2 O=HClO+OH-。常温下,该水解反应的平衡常数为K=1.0×10-6mol·L-1,则1.0mol· L -1NaCIO溶液的pH=________。
(3)工业上利用氨气生产氢氰酸(HCN)的反应为:CH4(g)+NH3(g) ![]() HCN(g)+3H2 (g) △H>O
HCN(g)+3H2 (g) △H>O
①其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图所示。X代表的是________(填“温度”或“压强”)。

②其他条件一定,向2L密闭容器中加人 n mol CH4和2 mol NH3,平衡时NH3体积分数随n变化的关系如图所示。若反应从开始到a点所用时间为10min,该时间段内用CH4的浓度变化表示的反应速率为________mol·L-1·min-1;平衡常数:K(a) ________K(b)(填“>”“=”或“<”)
③工业上用电解法处理含氰电镀废水(pH=10)的装置如图所示。

阳极产生的氯气与碱性溶液反应生成ClO-,ClO-将CN-氧化的离子方程式为:_____CN-+ _____ClO-+ ________====_____CO32-+_____N2↑+________+________若电解处理2 mol CN-,则阴极产生气体的体积(标准状况下)为________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据部分短周期元素的信息回答问题。
元素 | 元素信息 |
| 第3周期ⅥA族 |
| 族序数是周期数的3倍 |
| 原子序数是11 |
|
|
(1)![]() 、
、![]() 的元素符号分别为______、______,
的元素符号分别为______、______,![]() 、
、![]() 的元素名称分别为______、______。
的元素名称分别为______、______。
(2)写出![]() 、
、![]() 的常见单质在加热时的反应方程式:______。
的常见单质在加热时的反应方程式:______。
(3)从原子结构的角度分析,![]() 原子与
原子与![]() 原子的______相同,
原子的______相同,![]() 原子与
原子与![]() 原子的______相同。
原子的______相同。
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸铵[(NH4)2C2O4]为无色柱状晶体,不稳定,受热易分解,可用于测定Ca2+、Mg2+的含量。
I.某同学利用如图所示实验装置检验草酸铵的分解产物。
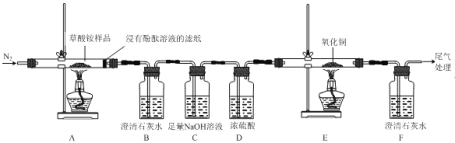
(1)实验证明草酸铵分解产物有:NH3、CO2、CO和水,其中说明分解产物中有CO的实验现象是__。
(2)装置C中发生反应的离子方程式为_____。
Ⅱ.该同学利用草酸铵测定某品牌牛奶中钙的含量,实验步骤如下:
①取100 mL牛奶,加入足量的草酸铵[(NH4)2C2O4]溶液,使牛奶中的钙转化成难溶的CaC2O4沉淀;
②过滤,用适量的蒸馏水洗涤沉淀表面吸附的少量(NH4)2C2O4、蛋白质等杂质;
③将沉淀转移至锥形瓶中,加足量的稀硫酸溶液溶解CaC2O4;
④然后以0.100mol·L-1的KMnO4溶液滴定生成的H2C2O4溶液,共消耗KMnO4溶液16.00mL。
已知:H++![]() +H2C2O4——Mn2++CO2+H2O(未配平)
+H2C2O4——Mn2++CO2+H2O(未配平)
(3)计算该品牌牛奶中钙的含量(单位:g·L-1),写出计算过程_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用分类的方法和氧化还原反应的规律,能实现某些物质的转化。
(1)请从下列试剂中选择合适的试剂完成指定转化(试剂可以重复选择)。
试剂:Cl2、HCl、Na2S、H2O;
①I2→IO3-的离子方程式:____;
②CuSO4→Na2SO4的化学方程式:_____。
(2)利用水钴矿(主要成分是Co2O3,含少量Fe2O3、Al2O3)制取CoC2O4·2H2O的流程如下:
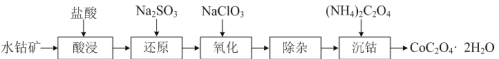
①“还原”时,Fe3+和Co3+均被还原为正二价阳离子,写出Co3+被还原的离子方程式_。
②“氧化”反应的离子方程式为:____。
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极电解AgNO3溶液,说法不正确的是( )
A.电解过程中阴极质量不断增加
B.电解过程中溶液的pH不断降低
C.此时向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解后两极产生的气体体积比为2∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.甘油醛(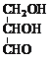 )和葡萄糖均属于单糖,互为同系物
)和葡萄糖均属于单糖,互为同系物
B.2,3,5,5四甲基3,3二乙基己烷的键线式为![]()
C.高聚物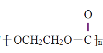 和
和![]() 均是缩聚产物,它们有共同的单体
均是缩聚产物,它们有共同的单体
D.将总物质的量为1 mol的水杨酸、1,2二氯乙烷和CH3NHCOOCH3的混合物与NaOH溶液充分反应,最多可以消耗2 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com