
科目: 来源: 题型:
【题目】2012年11月某白酒企业生产的白酒被曝塑化剂超标267%,白酒产品中的塑化剂主要源于塑料接酒桶、塑料输酒管、成品酒塑料内盖等。塑化剂DEHP的合成线路如下:
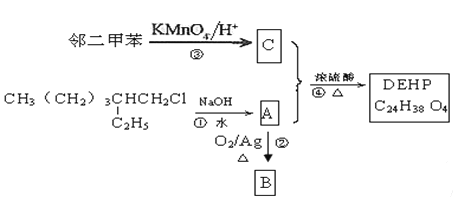
(1)A用系统命名法命名为______________,C分子核磁共振谱中显示有__________种不同化学环境的氢原子。C在一定条件下与乙二醇反应生成的高聚物是一种重要的合成纤维,俗称涤纶,其结构简式是__________。
(2)B含有的官能团名称为__________,①、②的反应类型分别为_______、_______。
(3)写出满足下列条件的C的同分异构体的结构简式:____________。
a.是苯的邻位二元取代物;b.遇FeCl3溶液显示特征颜色;
c.能与碳酸氢钠溶液反应
(4)写出下列反应的化学方程式:
反应②:_______________________________________________;
反应④:_______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯吡格雷![]() 是一种血小板凝固抑制剂,其合成路线如图:
是一种血小板凝固抑制剂,其合成路线如图:
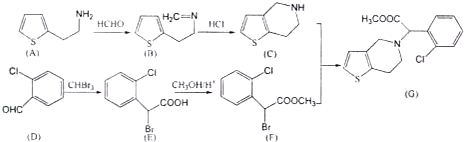
回答下列问题:
![]() 化合物D和F中的含氧官能团分别为 ______ 和 ______
化合物D和F中的含氧官能团分别为 ______ 和 ______ ![]() 填名称
填名称![]() .
.
![]() 有机反应类型:
有机反应类型:![]() : ______ ;
: ______ ;![]() : ______ .
: ______ .
![]() 反应
反应![]() 的化学方程式 ______ .
的化学方程式 ______ .
![]() 化合物
化合物![]()
![]()
![]() 是D的一种同系物,在H的同分异构体中,同时满足下列条件的物质的结构简式为 ______ .
是D的一种同系物,在H的同分异构体中,同时满足下列条件的物质的结构简式为 ______ .
![]() 分子中只含1个环,且有4中不同环境的H;
分子中只含1个环,且有4中不同环境的H;![]() 可与
可与![]() 溶液发生显色反应.
溶液发生显色反应.
![]() 根据已有知识,并结合本题信息,以
根据已有知识,并结合本题信息,以![]() 为起始原料,其他试剂任选,设计制备化合物
为起始原料,其他试剂任选,设计制备化合物 的合成路线图. ______
的合成路线图. ______
合成路线图示例如下:![]() .
.
查看答案和解析>>
科目: 来源: 题型:
【题目】将NaHCO3和Na2O2的固体混合物x g在密闭容器中加热至250℃,充分反应后排出气体.将反应后的固体溶入水无气体放出,再逐滴加入盐酸,产生气体(标准状况)与所加盐酸体积之间的关系如图所示.下列说法错误的是( )

A.HCl的浓度0.2mol/L
B.反应后固体的成分为NaOH与Na2CO3
C.密闭容器中排出气体的成分为O2和H2O
D.x的数值为6.09
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组设计如图所示的装置进行原电池原理的探究。下列叙述错误的是

A. a和b不连接时,锌片上有气体生成,该装置不能形成原电池
B. a和b用导线连接时铜片为正极,发生的反应式为:2H++2e-=H2↑
C. a和b用导线连接时,电子由Zn经导线流向Cu,再经稀硫酸流回Zn
D. 无论a和b是否连接,稀硫酸均参与反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分。请回答下列问题:

(1)上述元素中,属于s区的是__________ (填元素符号)。
(2)写出元素⑨的基态原子的价电子排布图________。
(3)元素的第一电离能:③________④(选填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为________;该分子为________分子(选填“极性”或“非极性”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据反应:2Ag+ + Cu = Cu2+ + 2Ag,设计如图所示原电池,下列说法错误的是( )。
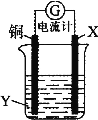
A.X可以是银或石墨
B.Y是硫酸铜溶液
C.电子从铜电极经外电路流向X电极
D.X极上的电极反应式为Ag+ + e-= Ag
查看答案和解析>>
科目: 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
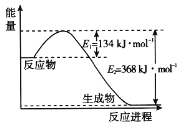
(1)图是1 mol NO2和1 mol CO反应生成CO2 和NO过程中的能量变化示意图,请写出NO2 和CO反应的热化学方程式______________________。
(2)在0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如下表:
T/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5 |
请回答下列问题:
①试比较K1、K2的大小,K1_________K2(填”>”“=“或”<”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是_________(填序号字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v正(N2)=3v逆(H2)
c.容器内压强保持不变 d.混合气体的密度保持不变
③400℃时,反应2NH3(g) ![]() N2(g)+3H2(g)的平衡常数K为______。当测得NH3、N2、H2的浓度分别为3 mol L1、2 mol L1、1 mol L1时,则该反应的v正(N2)____v逆(N2)(填”>”“=“或”<”)
N2(g)+3H2(g)的平衡常数K为______。当测得NH3、N2、H2的浓度分别为3 mol L1、2 mol L1、1 mol L1时,则该反应的v正(N2)____v逆(N2)(填”>”“=“或”<”)
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[一lg c(M2+)]与溶液pH的变化关系如图所示,已知该温度下,Ksp[Cu(OH)2]2],下列说法正确的是 ( )
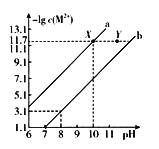
A. b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中:C(Fe2+):C(Cu2+):1:104.6
C. 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液
D. 除去CuSO4溶液中含有的少量Fe2+,可加入适量Cu0
查看答案和解析>>
科目: 来源: 题型:
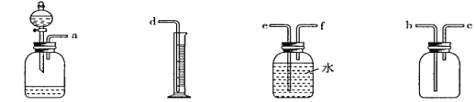
【题目】镁铝合金具有良好的强度、刚性、优良的电磁屏蔽性和导热性,使之成为笔记本电脑和轻薄手机的首选外壳材料。为测定某手机外壳镁铝合金中镁和铝的含最,并回收镁铝,某实验小组设计如下实验方案。
①除去手机外壳的涂层,剪其中一小块,称取其质量;
②组装仪器,检查气密性,用足盘稀盐酸溶解合金;
③测量产生气体的体积,计算结果;
④利用下列流程,从溶解合金后的溶液中回收分离镁铝。
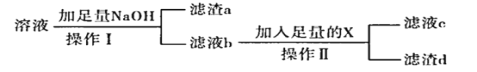
(1)请利用下图给定的仪器组成一套实验装置(每个仪器只能使用一次,可不选用)。各种仪器连接的先后顺序(用小写字母表示)_______
(2)除了测定产生气体的体积外,还应测定_______。
(3)回收流程中,操作I需要的玻璃仪器有烧杯、玻璃棒和_______,为保证回收产品的纯度,操作I后应_______。
(4)滤液b的溶质是_______(填化学式),试剂X是_______。
(5)向滤渣a中加入盐酸,产物是_______(填化学式),若从晶体中获得金属,应进行的操作是_______。
(6)若从除去涂层的手机壳上取样品mg加入足量盐酸后,测得产生的气体nL,实验条件下的气体摩尔体积为VmL/mol,则合金中Mg的质量为________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂—KNO3的U形管)构成一个原电池(如图)。以下有关该原电池的叙述正确的是( )
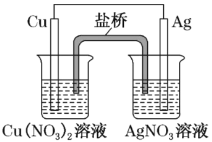
①在外电路中,电流由铜电极流向银电极;
②正极反应为Ag++e-=Ag;
③实验过程中取出盐桥,原电池仍继续工作;
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同;
A.①②B.③④C.②④D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com