
科目: 来源: 题型:
【题目】标准状况下有①6.72L甲烷②3.01×1023个氯化氢分子③13.6 g硫化氢④0.2 mol NH3。下列对这四种气体的关系从小到大表示不正确的是
A.体积:④<①<②<③B.密度:①<④<③<②
C.质量:④<①<③<②D.氢原子数:②<④<③<①
查看答案和解析>>
科目: 来源: 题型:
【题目】用含锌废渣(主要含Zn以及少量S、Fe、Mn、Cd等)制取氧化锌(ZnO)的工艺流程如图
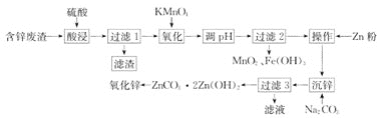
回答下列问题:
(1)“酸浸”时,锌、铁的浸出率如图(a)所示,应控制浸取终点的pH为________。
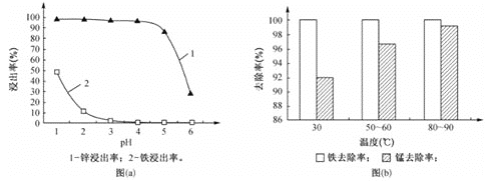
(2)“氧化”时,Fe2+、Mn2+去除率与温度的关系如图(b)所示,相同条件下还原性较强的是________(填“Fe2+”或“Mn2+”),Fe2+被KMnO4氧化生成Fe3+和MnO2的离子方程式为________。
(3)加Zn粉“操作”的目的是________。
(4)“沉锌”的离子方程式为________,由碱式碳酸锌制备轻质氧化锌的方法是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】G是药物合成中的一种重要中间体,下面是G的一种合成路线:
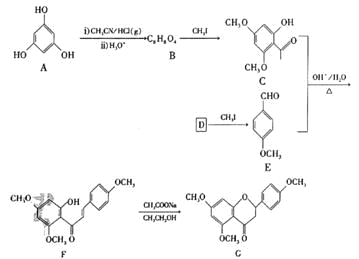
已知:![]()
![]()
 或
或![]()
回答下列问题:
![]() 的结构简式为________,其中所含官能团的名称为_______;B生成C的反应类型为_______。
的结构简式为________,其中所含官能团的名称为_______;B生成C的反应类型为_______。
![]() 的名称是________。
的名称是________。
![]() 由C和E合成F的化学方程式为________。
由C和E合成F的化学方程式为________。
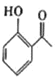
![]() 的同分异构体中,能发生银镜反应且分子结构中含苯环的还有________种,其中核磁共振氢谱上有6组峰,峰面积之比为
的同分异构体中,能发生银镜反应且分子结构中含苯环的还有________种,其中核磁共振氢谱上有6组峰,峰面积之比为![]() 的同分异构体的结构简式为________
的同分异构体的结构简式为________![]() 写出一种即可
写出一种即可![]() 。
。
![]() 参照上述合成路线,以
参照上述合成路线,以![]() 为原料
为原料![]() 其他试剂任选
其他试剂任选![]() ,设计制备巴豆醛
,设计制备巴豆醛![]() 的合成路线________。
的合成路线________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各有机物无论二者以什么比例混合,只要总物质的量一定,则完全燃烧生成H2O的质量和消耗氧气的质量不变的是( )
① 丙烷、丁炔 ② 丙烯、C4H6O2 ③ 乙炔、苯 ④ 甲醇、C3H4O5
A.①③B.①②C.②④D.③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案中不能达到相应实验目的的是:
A | B | C | D | |
方案 |
| 在2mL1mol/LNaOH溶液中,加入5滴1mol/L氯化镁溶液,有白色沉淀,再加入5滴氯化铁溶液,观察沉淀颜色 | 实验室制备氢气,用粗锌代替纯锌与稀硫酸反应,反应速率加快 |
|
目的 | 探究浓度对化学反应速率的影响 | 探究沉淀溶解平衡的移动 | 探究形成原电池对反应速率的影响 | 探究温度对化学平衡的影响 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,将0.1 mol/L的NaOH溶液滴入盛有50 mLpH=2 的HA溶液的绝热容器中,加入NaOH溶液的体积V与溶液温度T的关系如图。下列说法正确的是( )

A.a点溶液中,c(A-)+c(HA)=0.08 mol/L
B.b点溶液中,c(A-)<c(Na+)
C.a→b的过程中,发生了吸热反应
D.溶液中HA的电离平衡常数a点等于b点
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,发生反应3A(g)+2B(g)![]() 4C(s)+2D(g),加入4molA和2molB,2min后达到平衡,测得生成1.6mol C,则下列说法正确的是:
4C(s)+2D(g),加入4molA和2molB,2min后达到平衡,测得生成1.6mol C,则下列说法正确的是:
A.该反应的化学平衡常数表达式是K=![]()
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.若向平衡体系移走部分D,则此时正反应速率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】以NA表示阿伏加德罗常数,下列说法中正确的是( )
A. 53g碳酸钠中含NA个CO32—B. 0.1molOH—含NA电子
C. 1.8g重水(D2O)中含NA个中子D. 标准状况下11.2L臭氧(O3)中含NA个氧原子
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家借助自主研制的新型钨钴铁合金催化剂攻克了单壁碳纳米管结构的可控制备难题。海底金属软泥是在海底覆盖着的一层红棕色沉积物,蕴藏着大量的金属资源,含有钨、铁、锰、锌、钴等。
(1)基态钴原子的核外未成对电子数为__________。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为__________。
(2)纳米结构氧化钴可在室温下将甲硫醛(CH2S)完全催化氧化,甲醛分子属__________(填“极性”或“非极性”)分子,其中心原子的VSEPR构型为__________。
(3)六羰基钨[W(CO)6]的熔点为172℃,是一种重要的无机金属配合物,可溶于多数有机溶剂。三种组成元素的电负性由大到小的顺序为 __________(用元素符号表示)。配体CO中与W形成配位键的原子是C而不是O,原因是 ____________。
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是 ____________(填字母)。
A.苯 B.二氧化硫 C.四氯化碳 D.环己烷
(5) Fe2+、Fe3+能与CN-形成络离子,其晶胞结构如图1所示。该离子可形成铁蓝钾盐,该钾盐的化学式为___________。
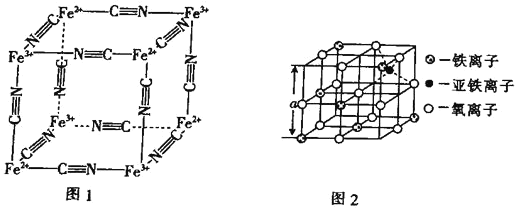
(6)图2是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,该立方体是不是Fe3O4的晶胞__________(填“是”或“否”);立方体中铁离子处于氧离子围成的 _________(填空间结构)空隙;根据上图计算Fe3O4晶体的密度为 ________gcm-3。(图中a=0.42nm,计算结果保留两位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】金合欢醇广泛应用于多种香型的香精中,其结构简式如图所示。下列说法不正确的是( )
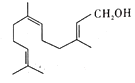
A.金合欢醇的同分异构体中不可能有芳香烃类
B.金合欢醇可发生加成反应、取代反应、氧化反应
C.金合欢醇分子的分子式为C15H26O
D.1 mol金合欢醇与足量Na反应生成0.5 mal氢气,与足量NaHCO3溶液反应生成1 mol CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com