
科目: 来源: 题型:
【题目】氰(CN)2的结构简式为N≡C—C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间。下列有关反应的化学方程式不正确的是( )
A. (CN)2+H2=2HCN
B. MnO2+4HCN=Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合液中通入少量Cl2:Cl2+2KCN=2KCl+(CN)2
查看答案和解析>>
科目: 来源: 题型:
【题目】元素![]() 、
、![]() 、
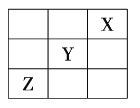
、![]() 在周期表中的相对位置如图所示。已知
在周期表中的相对位置如图所示。已知![]() 元素原子的外围电子排布式为
元素原子的外围电子排布式为![]() ,则下列说法不正确的是( )
,则下列说法不正确的是( )
A.![]() 元素原子的价电子排布式为
元素原子的价电子排布式为![]()
B.![]() 元素在元素周期表的第三周期第ⅥA族
元素在元素周期表的第三周期第ⅥA族
C.![]() 元素所在周期中所含非金属元素最多
元素所在周期中所含非金属元素最多
D.![]() 元素原子的核外电子排布式为
元素原子的核外电子排布式为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
![]()
项目 | 相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
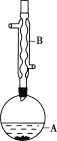
实验步骤:
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯3.9g。
回答下列问题:
(1)仪器B的名称是___。
(2)在洗涤操作中,第一次水洗和第二次水洗的主要目的分别是___。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后__(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)实验中加入少量无水MgSO4的目的是___。
(5)本实验的产率是___(填标号)。
a.30% b.40% c.60% d.90%
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于热化学方程式的说法正确的是
A. H2的燃烧热为285.8 kJ·mol1,则表示H2燃烧的热化学方程式可表示为:H2(g)+ ![]() O2
O2![]() H2O(g) ΔH=285.8 kJ·mol1
H2O(g) ΔH=285.8 kJ·mol1
B. 中和热为57.3 kJ·mol1,则NaOH与醋酸反应的中和热可以表示如下:NaOH(aq)+CH3COOH(aq)![]() CH3COONa(aq)+H2O(l) ΔH=57.3 kJ·mol1
CH3COONa(aq)+H2O(l) ΔH=57.3 kJ·mol1
C. 已知:C(s,金刚石)+O2(g)![]() CO2(g) ΔH=395.4 kJ·mol1,C(s,石墨)+O2(g)
CO2(g) ΔH=395.4 kJ·mol1,C(s,石墨)+O2(g)![]() CO2(g) ΔH=393.5 kJ·mol1,则C(s,金刚石)
CO2(g) ΔH=393.5 kJ·mol1,则C(s,金刚石)![]() C(s,石墨)ΔH=1.9 kJ·mol1
C(s,石墨)ΔH=1.9 kJ·mol1
D. 已知1 mol CH4完全燃烧生成CO2和液态水放出890.4 kJ的热量,则该反应中转移1 mol电子时放出的热量为222.6 kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是元素周期表前四周期的一部分,下列有关R、W、X、 Y、Z五种元素的叙述中,正确的是( )
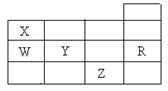
A. 通常情况下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. W的电负性比X的的电负性大
D. 第一电离能:R>W>Y
查看答案和解析>>
科目: 来源: 题型:
【题目】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量硫酸铁、硫酸亚铁固体,均配制成100mL0.1mol/L的溶液。在配制FeSO4溶液时需加入少量铁屑,其目的是__。
(2)甲组同学取2mLFeSO4溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeSO4溶液与氯水反应的离子方程式为___。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeSO4溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是__。
(4)丙组同学研究pH对FeSO4稳定性的影响,得到如图所示结果,增强Fe2+稳定性的措施为__。(写出一条即可)
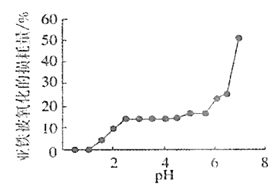
(5)丁组同学为了探究Fe2(SO4)3与Cu的反应,做了如图所示实验:

①Fe3+与Cu反应的离子方程式为__。
②为了探究白色沉淀产生的原因,同学们查阅资料得知:
i.CuSCN是难溶于水的白色固体;
ii.SCN的化学性质与I-相似;
ii.2Cu2++4I-=2CuI↓+I2。
填写实验方案:
实验方案 | 现象 |
步骤1:取4mL0.2mol/L的FeSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液。 | 无明显现象 |
步骤2:取4mL_mol/L的CuSO4溶液,向其中滴加3滴0.1mol/L的KSCN溶液。 | 产生白色沉淀 |
Cu2+与SCN-反应的离子方程式为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验需要500mL0.10mol/L的Na2CO3溶液,现通过如下步骤配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水搅拌溶解;
②用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
③盖好瓶塞,反复上下颠倒,摇匀;
④把溶解固体后所得溶液冷却至室温,转入仪器A中;
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切;
(1)操作步骤的正确顺序为__(填序号)。
(2)称量的Na2CO3固体质量应为__g。
(3)仪器A的名称是__。
(4)取出100mL配制好的溶液,加蒸馏水稀释至c(Na2CO3)=0.02mol/L。则稀释后溶液的体积为__。
(5)下列关于容量瓶的使用方法中,正确的是__(填字母序号)。
A.使用前要检验是否漏水
B.在容量瓶中直接溶解固体或稀释液体
C.在烧杯中溶解固体后,迅速将溶液转移到容量瓶中
D.向容量瓶中转移溶液用玻璃棒引流
E.加水时水量超过了刻度线,迅速用胶头滴管将过量的水吸出
(6)下列操作会使所配溶液的物质的量浓度偏低的是__(填字母序号)。
A.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
B.定容读数时,俯视容量瓶上的刻度线
C.加水定容时,水量超过了刻度线
D.洗涤步骤中,洗涤液没有转入容量瓶
查看答案和解析>>
科目: 来源: 题型:
【题目】用CaSO4代替O2与燃料CO反应是一种高效、清洁的新型燃烧技术,发生如下反应:
①![]() CaSO4(s)+CO(g)
CaSO4(s)+CO(g) ![]() CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
②CaSO4(s)+CO(g) CaO(s)+CO2(g)+SO2(g) ΔH2=+210.5 kJ·mol-1
③CO(g) ![]() C(s)+
C(s)+![]() CO2(g) ΔH3=-86.2 kJ·mol-1
CO2(g) ΔH3=-86.2 kJ·mol-1
下列说法错误的是 ( )
A. 反应①达到平衡时,增大压强平衡不移动
B. 反应②的平衡常数表达式为K=![]()
C. 反应①和②是主反应,反应③是副反应
D. 2CaSO4(s)+7CO(g) ![]() CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)是放热反应
CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)是放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】用化学用语表达。
(1)小苏打受热易分解,化学方程式为__。
(2)金属钠着火不能用水扑灭,用离子方程式解释其原因__。
(3)工业上用氯气和熟石灰制备漂白粉,化学方程式为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组将如图所示装置按一定顺序连接,在实验室里制取一定量的![]() 所通气体过量并充分反应
所通气体过量并充分反应![]() 。请回答下列问题:
。请回答下列问题:
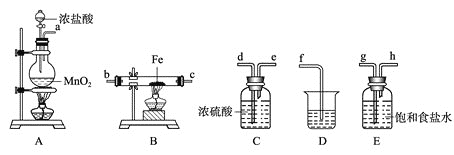
![]() 中发生反应的化学方程式为_____________________。
中发生反应的化学方程式为_____________________。
![]() 各装置的正确连接顺序为
各装置的正确连接顺序为![]() 填写装置代号
填写装置代号![]() ____
____![]() ____
____![]() ____
____![]() 。
。
![]() 写出装置D中反应的离子方程式_____________________。
写出装置D中反应的离子方程式_____________________。
![]() 反应结束后,可以检验B中生成物中含有
反应结束后,可以检验B中生成物中含有![]() 的试剂是_______
的试剂是_______![]() 填写试剂名称
填写试剂名称![]() 。
。
![]() 该小组欲用如图所示装置收集尾气,并测量多余气体的体积。
该小组欲用如图所示装置收集尾气,并测量多余气体的体积。

![]() 若图中所示量气装置由干燥管、乳胶管和
若图中所示量气装置由干燥管、乳胶管和![]() 滴定管改造后组装而成,此处所用滴定管是_____________
滴定管改造后组装而成,此处所用滴定管是_____________![]() 填“酸式”或“碱式”
填“酸式”或“碱式”![]() 滴定管。
滴定管。
![]() 为提高测量的准确性,上图装置中的液体可用___________。
为提高测量的准确性,上图装置中的液体可用___________。
![]() 如果开始读数时操作正确,最后读数时俯视右边滴定管液面,会导致所测气体的体积_______
如果开始读数时操作正确,最后读数时俯视右边滴定管液面,会导致所测气体的体积_______![]() 填“偏大”、“偏小”或“无影响”
填“偏大”、“偏小”或“无影响”![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com