
科目: 来源: 题型:
【题目】关于下列各图的叙述错误的是![]()
化学方程式 | 平衡常数K |
|
|
|
|
|
|
|
|
A.已知1molCO燃烧放出的热为283kJ,![]() ;
;![]() 则
则 表示CO和
表示CO和![]() 生成
生成![]() 和
和![]() 的能量变化
的能量变化
B.常温下![]()
![]() HB溶液和
HB溶液和![]()
![]() 溶液等体积混合后溶液的
溶液等体积混合后溶液的![]() ,则混合溶液中离子浓度的大小顺序为:
,则混合溶液中离子浓度的大小顺序为:![]()
C.常温下,![]() 和
和![]() 反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时
反应生成HX的平衡常数如表所示,仅依据K的变化,就可以说明在相同条件下,平衡时![]() 从
从![]() 到
到![]() 的转化率逐减小,且HX的还原性逐渐减弱
的转化率逐减小,且HX的还原性逐渐减弱
D.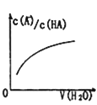 中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,
中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中, 的变化情况
的变化情况
查看答案和解析>>
科目: 来源: 题型:
【题目】已知![]() 。在含少量
。在含少量![]() 的溶液中,
的溶液中,![]() 分解反应过程为
分解反应过程为
i.![]()
ii.![]()
下列说法不正确的是
A. ![]()
B. ![]() 是
是![]() 分解反应的催化剂
分解反应的催化剂
C. 欲分解2mol![]() (l),至少需要提供
(l),至少需要提供![]() 的热量
的热量
D. 若生成![]() ,则反应ii转移电子的物质的量为
,则反应ii转移电子的物质的量为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】能源是人类生存和发展的重要支柱。研究和有效地开发新能源有重要意义。已知 CH3CH2CH2CH3(g)与 CH3CH(CH3)CH3(g)的燃烧过程如图所示:

已知:H2O(g)=H2O(l) ΔH=-41kJ·mol-1。请根据以上信息,回答下列有关问题:
(1)图形中 E 表示 CH3CH2CH2CH3(g)燃烧反应逆反应的_____。
(2)CH3CH2CH2CH3(g)与 CH3CH(CH3)CH3(g)的热稳定性_____更高。
(3)表示CH3CH(CH3)CH3(g)燃烧热的热化学方程式为_____。
(4)CH3CH2CH2CH3(g)转化为 CH3CH(CH3)CH3(g)的热化学反应方程式为_____
(5)如表所示是部分化学键的键能参数(已知CO的结构式为C≡O):

合成气(CO 和 H2 的混合气体)可以合成 CH3CH2CH2CH3(g),同时生成 H2O(g),则合成 1molCH3CH2CH2CH3(g)的 ΔH=__。
查看答案和解析>>
科目: 来源: 题型:
【题目】试用VSEPR理论判断下列分子或离子的立体构型,并判断中心原子的杂化类型:
(1)H2O____________形,杂化类型_________;
(2)CO32-__________形,杂化类型_________;
(3)SO32-__________形,杂化类型_________;
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应属于消去反应的是(反应条件省略)( )
A.![]() -CH3CH2OH →
-CH3CH2OH →![]() -CH2=CH2↑+ H2O
-CH2=CH2↑+ H2O
B.CH3CH2CH3 + Br2→CH3CH2CH2Br + HBr
C.CH3CH2CHO + H2→CH3CH2CH2OH
D.2CH3CH2CH2OH + 2O2→CH3CH2CHO + 2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】某班在实验室进行制取乙酸乙酯并对其性质进行探究的分组实验,主要步骤如下:
I.为探究乙酸乙酯的水解反应,某组同学取大小相同的3支试管,分别加入以下溶液,充分振荡,放在同一水浴加热相同时间,观察到如下现象。
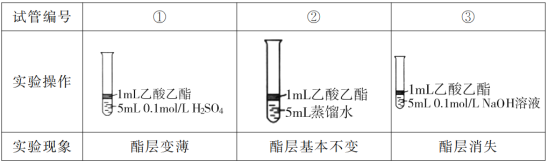
(1)设计实验①和②,是为了探究___对乙酸乙酯的水解的影响。
(2)试管③中反应的化学方程式是__。
Ⅱ.某组同学为验证醋酸、碳酸与苯酚三者酸性的强弱,经过慎重考虑,设计如下实验装置。已知A中装有醋酸,D中装有苯酚钠,请回答问题:
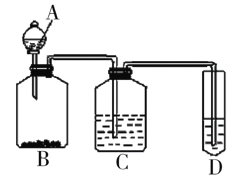
(1)C所盛放的药品是___,装置C的作用___。
(2)试描述能证明三种酸的酸性强弱的实验现象___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组在实验室用重晶石(主要成分BaSO4)对工业生产BaS进行模拟实验。BaS是可溶盐,在工业生产中,它是制备其他钡盐的中间产物。已知:
BaSO4(s)+4C(s)![]() 4CO(g)+BaS(s) ΔH1=+571.2 kJ·mol-1 ①
4CO(g)+BaS(s) ΔH1=+571.2 kJ·mol-1 ①
BaSO4(s)+2C(s)![]() 2CO2(g)+BaS(s) ΔH2=+226.2 kJ·mol-1 ②
2CO2(g)+BaS(s) ΔH2=+226.2 kJ·mol-1 ②
下列说法不正确的是( )
A.上述反应中BaSO4均作氧化剂
B.反应C(g)+CO2(g)![]() 2CO(g)的ΔH3>+172.5 kJ·mol-1
2CO(g)的ΔH3>+172.5 kJ·mol-1
C.实际生产中必须加入过量的炭使BaSO4得到充分的还原,同时还要通入空气,因为①②为吸热反应,炭和氧气反应放热维持反应所需高温
D.以BaS作为沉淀剂,用于铅和汞沉淀的转化
查看答案和解析>>
科目: 来源: 题型:
【题目】元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y为地壳中含量最多的元素,M原子的最外层电子数与次外层电数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,请回答下列问题:
(1)M在元素周期表中的位置__;Z+离子的结构示意图为__。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式__。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__。
(4)实验室制备R的单质,该反应的离子方程式为__。
(5)R非金属性强于M,下列选项中能证明这一事实的是__(填字母序号)。
A.常温下的R单质熔沸点比M单质的高
B.R的氢化物比M的氢化物更稳定
C.一定条件下R和M的单质都能与NaOH溶液反应
D.最高价氧化物对应水化物的酸性强弱:R>M
(6)由X、Y、Z、M四种元素组成的一种弱酸酸式盐A。向A溶液中通入氯气,得到无色溶液,写出该反应的离子方程式__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列中心原子的杂化轨道类型和分子几何构型不正确的是( )
A.PCl3中 P原子sp3杂化,为三角锥形
B.BCl3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp杂化,为直线形
D.H2S中S原子sp杂化,为直线形
查看答案和解析>>
科目: 来源: 题型:
【题目】含氟的卤素互化物通常作氟化剂,使金属氧化物转化为氟化物,如2Co3O4+6C1F3= 6CoF3+3C12+4X。下列有关该反应的说法,正确的是
A. X与O3互为同位素 B. ClF3中氯元素为-3价
C. Co3O4在反应中作氧化剂 D. lmol Co3O4参加反应转移9 mol电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com