
科目: 来源: 题型:
【题目】以淀粉和油脂为原料,制备生活中的某些物质。
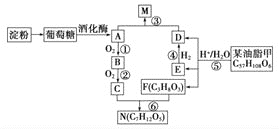
已知:反应![]() 生成D、E、F的物质的量之比为
生成D、E、F的物质的量之比为![]() ,E与等物质的量的
,E与等物质的量的![]() 反应生成D。请回答下列问题:
反应生成D。请回答下列问题:
![]() 葡萄糖的分子式为________,C分子中官能团的名称为________。
葡萄糖的分子式为________,C分子中官能团的名称为________。
![]() 下列说法正确的是________。
下列说法正确的是________。
A.淀粉、油脂都是高分子化合物,都能发生水解反应
B.C、D属于同系物;M、N也属于同系物
C.上述![]() 中属于取代反应的为
中属于取代反应的为![]()
D.B、E含不同官能团,但都能使酸性高锰酸钾溶液褪色
![]() 写出N的一种结构简式:_________________________;C与F按不同的比例反应,还可以生成另外两种物质X、Y,且相对分子质量
写出N的一种结构简式:_________________________;C与F按不同的比例反应,还可以生成另外两种物质X、Y,且相对分子质量![]() ,则Y的分子式为________。
,则Y的分子式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究物质结构与性质之间的关系和元素性质的递变规律,设计了如下系列实验。回答下列问题:
I.NaNH2熔点(210℃)比NaOH 熔点(318.4℃)低, 解释原因正确的是 (__________)
A.是因为NaNH2比NaOH 的相对分子质量小,前者分子间作用力小。
B.NaOH存在分子间氢键
C.NaNH2、NaOH均是离子化合物,其熔沸点高低与离子键的强弱有关,阴、阳离子电荷数越高,离子半径越小,离子键强度越大(或离子晶体的晶格能越大),则熔点越高。由于原子半径N>O,且NH2- 比OH- 原子个数多,则NH2- 比OH- 离子半径大,所以NaNH2比NaOH离子晶体的晶格能小,其熔点低。
D.N和O均处于第二周期,N在左方,同周期元素从左到右,元素的非金属性增强,其氢化物水溶液的酸性H2O>NH3,则碱性NaNH2>NaOH
II.根据下图所示装置回答以下问题。

(1)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证Cl的非金属性大于S:锥形瓶中发生反应的离子方程式为_________________________。试管中的实验现象为___________________________。
(2)若要用此装置证明非金属性: N>C>Si,从以下所给物质中选出实验所要用到物质:
①稀HNO3溶液 ②稀硫酸溶液 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
试剂A与C分别对应为_________________(填数字序号)。
有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为发生干扰的化学方程式为:_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物(X)的结构简式如下图,下列关于它的说法不正确的是( )
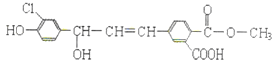
A.X遇FeCl3溶液能发生显色反应
B.一定条件下,X能发生取代、水解、氧化、加成、加聚等反应
C.1mol X分别与足量的NaOH、氢气反应,最多能消耗4mol NaOH 、7mol 氢气
D.等物质的量的该有机物分别与足量的Na、NaHCO3反应时,则消耗Na、NaHCO3的物质的量之比是3:1
查看答案和解析>>
科目: 来源: 题型:
【题目】锌—空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH+2H2O![]() Zn(OH)42-。下列说法不正确的是( )
Zn(OH)42-。下列说法不正确的是( )
A. 充电时,电解质溶液中K+向阴极移动
B. 充电时,电解质溶液中c(OH)逐渐增大
C. 放电时,负极反应为:Zn+4OH2e=Zn(OH)42-
D. 放电时,电路中通过2 mol电子,消耗氧气11.2 L
查看答案和解析>>
科目: 来源: 题型:
【题目】向![]() 溶液中,逐渐加入铁粉至过量
溶液中,逐渐加入铁粉至过量![]() 假设生成的气体只有一种
假设生成的气体只有一种![]() ,在此过程中,
,在此过程中,![]() 随
随![]() 变化如图所示,试回答下列问题:
变化如图所示,试回答下列问题:
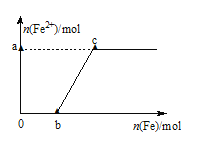
(1)写出![]() 段的离子方程式:_______________。
段的离子方程式:_______________。
(2)a=__________,![]() ___________;
___________;
(3)写出向c点处的反应液中加入稀盐酸后的离子方程式:________________。
(4)当加入铁粉nmol时![]() ,溶液中Fe
,溶液中Fe![]() 的物质的量为_____________
的物质的量为_____________![]() 用含n的式子表示
用含n的式子表示![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为2H2+O2═2H2O,下列有关说法正确的是( )
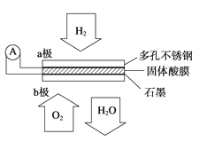
A. 电流通过外电路从a极流向b极
B. b极上的电极反应式为O2+2H2O+4e-═4OH-
C. 每转移0.2 mol电子,在负极上消耗标况下1.12 L的O2
D. H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以钛铁矿[主要成分为钛酸亚铁( FeTiO3),含有MgO、SiO2等杂质]为原料,制备金属钛和铁红的工艺流程如下:

已知:①酸浸时, FeTiO3转化为Fe2+和TiO2+;②本实验温度下,Ksp[Mg(OH)2]=1.0×10-11;请回答下列问题:
(1)酸浸时如何提高浸取速度和浸取率_____________________________(至少答两种方法)。
(2)“水解”生成H2TiO3的离子方程式为_________________________。
(3)“沉铁”过程中,气态产物的电子式为__________________;该过程需控制反应温度低于35 ℃,原因为___________________________________________________。
(4)滤液3可用于制备Mg(OH)2。若滤液3中c(Mg2+)=1.0×10-3 mo/L,向其中加入NaOH固体,调整溶液pH值大于________时,可使Mg2+沉淀完全。
(5)“电解”时,电解质为熔融的CaO,两电极材料为石墨棒。则_______极石墨棒需要定期更换,原因是__________________________________________________________。
(6)测定铁红产品纯度:称取m g铁红,溶于一定量的硫酸之中,配成500.00 mL溶液。从其中量取20.00 mL溶液,加入过量的KI,充分反应后,用 c mol/L硫代硫酸钠(Na2S2O3)标准液滴定至终点,发生反应:I2+2S2O![]() ===S4O
===S4O![]() +2I-。平行滴定三次,硫代硫酸钠平均消耗体积为V mL。则铁红产品的纯度为________(用c、V、m表示)。
+2I-。平行滴定三次,硫代硫酸钠平均消耗体积为V mL。则铁红产品的纯度为________(用c、V、m表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是
①CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol1
CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol1
②CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=890.3 kJ·mol1
CO2(g)+2H2O(l) ΔH=890.3 kJ·mol1
③CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=890.3 kJ·mol1
CO2(g)+2H2O(g) ΔH=890.3 kJ·mol1
④2H2(g)+O2(g)![]() 2H2O(l) ΔH=571.6 kJ·mol1
2H2O(l) ΔH=571.6 kJ·mol1
A. 仅有② B. 仅有②④ C. 仅有②③④ D. 全部符合要求
查看答案和解析>>
科目: 来源: 题型:
【题目】溴苯是无色油状液体,具有苯的气味。化工上主要用于溶剂、分析试剂和有机合成等。某化学小组欲利用如图所示的装置通过实验探究:
Ⅰ.苯与液溴发生取代反应:已知:MnO2+2NaBr+2H2SO4![]() Br2↑+MnSO4+Na2SO4+2H2O
Br2↑+MnSO4+Na2SO4+2H2O

(1)仪器X的名称______________ ,实验室制备溴苯的化学方程式为____________________;
这样制取的溴苯中会溶解过量的Br2 ,可以用________洗涤除Br2。
A.Na2SO3溶液 B.H2O C.乙醇溶液 D.NaOH溶液
(2)制取溴苯的实验操作步骤如下:
①连接装置,其接口顺序为(填字母):d接________,________接________,________接c;
②检查装置的气密性;
③C中加入固体药品,滴加浓硫酸,再打开D处开关K,点燃C处酒精灯;将D装置中的铁丝插入混合液中,一段时间后,D中液体沸腾,原因是_____________________;
④关闭C中分液漏斗的旋塞。
(3)A中对广口瓶进行热水浴的目的_________________________________。
(4)若B中有淡黄色沉淀生成,能否确定苯与液溴发生了取代反应?________(答“能”或“否”)解释其中的原因_________________________________;
Ⅱ.探究苯与液溴在催化剂作用下的反应机理。
查阅文献:①Br+有强氧化性,可以和水分子发生氧化还原反应 ②苯与液溴在溴化铁催化下的反应机理共分三步:(填写下列空白)
第一步:Br2+FeBr3![]() Br++FeBr
Br++FeBr![]() 第二步:
第二步:![]()
请完成第三步反应:__________________________;该小组将A装置中浓硫酸替换成稀硫酸时实验失败,试从反应机理推测可能的原因是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
(1)铷位于元素周期表的第________周期________族。
(2)关于铷的下列说法中不正确的是________(填数字序号)。
①与水反应比钠更剧烈 ②Rb2O在空气中易吸收水和二氧化碳
③Rb2O2与水能剧烈反应并释放出O2
④它是极强的还原剂 ⑤RbOH的碱性比同浓度的NaOH弱
(3)现有铷和另一种碱金属形成的合金5 g,与足量水反应时生成标准状况下的气体2.24 L,则另一碱金属可能是_______________(填元素符号)。
(4)铷久置于空气中,最终变成产物是_____________。
A、Rb2O B、Rb2O2 C、Rb2CO3 D、RbHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com