
科目: 来源: 题型:
【题目】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是______(填字母)。
A.Na2O与水反应 B.甲烷的燃烧反应C.CaCO3受热分解 D.锌与盐酸反应
(2)获取能量变化的途径① 通过化学键的键能计算。已知:
化学键种类 | H—H | O=O | O—H |
键能(kJ/mol) | 436 | 498 | 463.4 |
计算可得:2H2(g)+ O2(g) =2H2O(g) H=____________kJ·mol-1
②通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+![]() O2(g) =Na2O(s)△H=-414kJ·mol-1
O2(g) =Na2O(s)△H=-414kJ·mol-1
Ⅱ.2Na(s)+O2(g) =Na2O2(s)△H=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式__________。
③ 利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入________(填序号)。
A.50 mL 0.50 mol·L-1NaOH溶液B.50 mL 0.55 mol·L-1NaOH溶液 C.1.0 g NaOH固体
查看答案和解析>>
科目: 来源: 题型:
【题目】有一无色透明溶液,欲确定是否含有下列离子:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,取该溶液的实验如下:
,取该溶液的实验如下:
实验步骤 | 实验现象 |
| 溶液变红色 |
| 有无色气体产生,气体遇空气可以变成红棕色 |
| 有白色沉淀生成 |
| 有稳定的白色沉淀生成,且不溶于稀硝酸 |
| 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
由此判断,下列说法正确的是![]()
A.根据实验![]() 可以确定溶液中不含有
可以确定溶液中不含有![]() 和
和![]() ,因为这二个离子相对应的酸为弱酸
,因为这二个离子相对应的酸为弱酸
B.溶液中一定存在的离子是![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ;溶液中肯定不存在的离子是:
;溶液中肯定不存在的离子是:![]() 、
、![]() 、
、![]() 、
、![]()
C.为进一步确定其它离子,应该补充焰色反应的实验来检验![]() 就可以
就可以
D.通过实验![]() 和
和![]() 就可以确定溶液中一定含有
就可以确定溶液中一定含有![]() ,一定不含有
,一定不含有![]() 、
、![]() 、
、![]() ,所以实验步骤
,所以实验步骤![]() 的设计是错误的
的设计是错误的
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中不正确的是
A.σ键比π键的电子云重叠程度大,形成的共价键强
B.s-sσ键与s-pσ键的电子云形状对称性相同
C.丙烯(CH3—CH=CH2)分子有8个σ键,1个π键,其中碳原子分别是sp2、sp3杂化
D.N2分子中有一个σ键,2个π键;NH4+中4个N-H键的键能不相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机化合物的说法正确的是![]()
A.医院里常用无水乙醇杀菌、消毒
B.乙醇和乙酸都能与NaOH溶液反应
C.乙酸乙酯中的乙酸可用饱和![]() 溶液除去
溶液除去
D.乙烯、聚乙烯和苯分子中均含有碳碳双键
查看答案和解析>>
科目: 来源: 题型:
【题目】硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为______________。
(2)锗、砷、硒的第一电离能大小排序为_______________。H2SeO4的酸性比H2SeO3的强,其原因是______________________。
(3)H2SeO3的中心原子杂化类型是_________;SeO32-的立体构型是___________。与SeO42-互为等电体的分子有(写一种物质的化学式即可)_______________。
(4)H2Se属于_________(填:极性或非极性)分子;单质硒的熔点为217℃,它属于________晶体。
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为____________;若该晶胞密度为ρgcm-3,硒化锌的摩尔质量为M g/mol。NA代表阿伏加德罗常数,则晶胞参数a为___________pm。
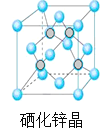
查看答案和解析>>
科目: 来源: 题型:
【题目】苯乙烷(C8H10)可生产塑料单体苯乙烯(C8H8),其反应原理是C8H10(g)![]() C8H8(g)+H2(g) ΔH=+125kJ·mol-1
C8H8(g)+H2(g) ΔH=+125kJ·mol-1
Ⅰ.某温度下,将0.40mol苯乙烷,充入2L真空密闭容器中发生反应,测定不同时间该容器内物质的量,得到数据如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 | n3 |
n(C8H8)/mol | 0.00 | 0.10 | n1 | 0.16 | 0.16 |
(1)该温度下,该反应的化学平衡常数K=________________。
(2)若保持其他条件不变,用0.40molH2(g)和0.40molC8H8(g)合成C8H10(g),当有30kJ热量放出时,该反应中H2的转化率是________________,通过计算说明此时,该反应是否达到了平衡状态__________?
查看答案和解析>>
科目: 来源: 题型:
【题目】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
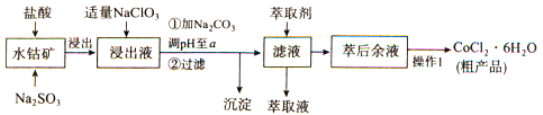
已知:①浸出液含有的阳离子主要有H+、CO2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
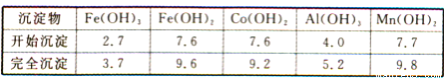
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式:_______________。
(2)若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式:_______________。
(3)“操作1”中包含3个基本实验操作,它们依次是_____________、__________和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是_____________。
(4)萃取剂对金属离子的萃取率与pH的关系如图向“滤液”中加入萃取剂的目的是____________,其使用的最佳pH范围是______。
A 2.0~2.5 B 3.0~3.5 C 4.0~4.5 D 5.0~5.5
(注:横坐标依次为1-6;单位:PH)
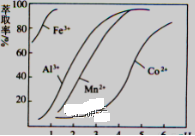
(5)为测定粗产品中CoCl2·6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是__________。(答一条即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中正确的是![]()
A.实验室欲配制![]() 的
的![]() 溶液,可用
溶液,可用![]() 胆矾及相应容器配制
胆矾及相应容器配制
B.将适量![]() 饱和溶液滴入沸水中并不断搅拌可制得氢氧化铁胶体
饱和溶液滴入沸水中并不断搅拌可制得氢氧化铁胶体
C.实验室中从海带里提取碘的过程是:灼烧![]() 溶解
溶解![]() 过滤
过滤![]() 萃取
萃取
D.用分液漏斗、烧杯、铁架台![]() 带铁圈
带铁圈![]() 、饱和
、饱和![]() 溶液可除去乙酸乙酯中的乙酸
溶液可除去乙酸乙酯中的乙酸
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活息息相关,下列说法不正确的是![]()
A.医用酒精的浓度通常为![]()
B.用食醋可除去热水壶内壁的水垢
C.烹鱼时加适量醋和酒可以增加香味
D.乙烯可作为水果的催熟剂
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)化合物A可由环戊烷经三步反应合成:
 (A)
(A)
已知:![]()
![]()

反应1的试剂与条件为_____;反应2的化学方程式为_____。
(2)如图是以环戊烷为原料制备环戊二烯的合成路线:
![]()
![]()
![]()
![]()
![]()
![]()

![]()
![]()
其中,反应②的反应试剂和条件是_____,反应③的反应类型是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com