
科目: 来源: 题型:
【题目】现有7瓶失去标签的试剂瓶,已知它们盛装的液体可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖溶液、蔗糖溶液。现通过如下实验来确定各试剂中所装液体的名称。
实验步骤和方法 | 实验现象 |
①把7瓶液体依次标号为A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
③分别取少量7种液体于试管中加新制的 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
④各取C、D、E少量于试管中,加稀 | 只有C中仍有分层现象,且在D的试管中闻到特殊香味 |
(1)试写出下列序号代表的液体名称:
A________,B________,C_______,D_______,E______,F______,G________。
(2)写出在D中加入![]() 溶液并加热的化学方程式:_______。
溶液并加热的化学方程式:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生称取9 g淀粉溶于水,测定淀粉水解的百分率,其过程如下(已知含有醛基的有机物可在碱性条件下与银氨溶液发生银镜反应生成单质Ag):

(1)填写各步所加试剂的名称:A.________;B.________;C._________。
(2)只加A而不加B是否可行?____(填“是”或“否”),理由是__________________________________。
(3)当析出2.16 g金属单质时,淀粉的水解率为___(已知1 mol醛基发生银镜反应时生成2 mol Ag)。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在10mL0.1mol·L1 Na2CO3溶液中逐滴加入0.1mol·L1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示,下列说法不正确的是

A.溶液的pH为7时,溶液的总体积大于20mL
B.在B点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-)+c(Cl-)
C.在A点所示的溶液中:c(Na+)=c(CO32-)=c(HCO3-)>c(OH-)>c(H+)
D.已知CO32-水解常数为2×10-4,当溶液中c(HCO3-)=2c(CO32-)时,溶液的pH=10
查看答案和解析>>
科目: 来源: 题型:
【题目】甲~庚等元素在周期表中的相对位置如下表,己的最高价氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数。下列判断正确的是( )
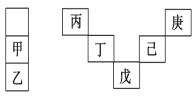
A.丙与戊的原子序数相差18
B.气态氢化物的稳定性:庚<己<戊
C.常温下,甲和乙的单质均能与水剧烈反应
D.丁的最高价氧化物可用于制造光导纤维
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20 mL0.010 mol·L-1的HA溶液中逐滴加入0.010 mol·L-1的NaOH溶液,溶液中c(OH-)与所加NaOH溶液的体积(V)的关系如图所示。下列说法不正确的是( )
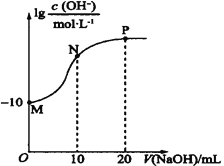
A.常温下,Ka(HA)≈1.0×10-6
B.N点溶液中存在:c(Na+)+c(H+)=c(A-)+c(OH-)
C.P点后的溶液中均存在:c(Na+)>c(A-)>c(OH-)>c(H+)
D.水的电离程度:M<N<P
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案设计及结论均正确的是( )
A.淀粉溶液![]() 水解液
水解液![]() 为蓝。结论:淀粉完全没有水解
为蓝。结论:淀粉完全没有水解
B.淀粉溶液![]() 水解液
水解液![]() 无砖红色沉淀。结论:淀粉完全水解
无砖红色沉淀。结论:淀粉完全水解
C.淀粉溶液![]() 水解液
水解液![]() 中和液
中和液![]() 有砖红色沉淀。结论:淀粉已水解
有砖红色沉淀。结论:淀粉已水解
D.淀粉溶液![]() 水解液
水解液![]() 无现象。结论:淀粉没有水解
无现象。结论:淀粉没有水解
查看答案和解析>>
科目: 来源: 题型:
【题目】某红色固体粉末样品可能含有![]() 和
和![]() 中的一种或两种,某化学兴趣小组对其组成进行探究.资料支持:
中的一种或两种,某化学兴趣小组对其组成进行探究.资料支持:![]() 在酸性溶液中会发生反应:
在酸性溶液中会发生反应:![]()
方案一:
(1)学生甲取少量样品于烧杯中,加入过量浓硝酸,产生一种红棕色的气体.由此可得出样品中一定含有____,写出产生上述气体的化学方程式___。
(2)进一步探究样品中另一种成分.实验操作步骤为:取少量上述溶液,___。
方案二:
(3)学生乙取少量样品于烧杯中,加入过量稀硫酸,并作出如下假设和判断,结论正确的是______。
A.若固体全部溶解,说明样品一定含有![]() ,一定不含有
,一定不含有![]()
B.若固体部分溶解,说明样品一定含有![]() ,一定不含有
,一定不含有![]()
C.若固体全部溶解,再滴加KSCN溶液,溶液不变红色,说明样品一定含有![]() 和
和![]()
方案三:学生丙利用如图所示装置进行实验,称量反应前后装置C中样品的质量,以确定样品的组成.回答下列问题:
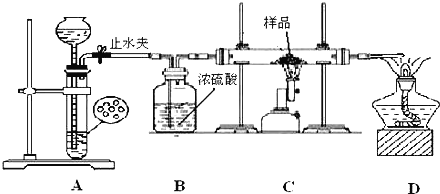
(4)装置A是氢气的发生装置,可以使用的药品是______。
A.氢氧化钠溶液和铝片 B.稀硝酸和铁片 C.稀硫酸和锌片 D.浓硫酸和镁片
(5)下列实验步骤的先后顺序是______(填序号)。
①打开止水夹; ②关闭止水夹; ③点燃C处的酒精喷灯;④熄灭C处的酒精喷灯 ⑤收集氢气并验纯
(6)假设样品全部参加反应,若实验前样品的质量为1.6克,实验后称得装置C中固体的质量为1.3克.则样品的组成是______。(可能用到的相对原子质量:Fe:56Cu:64C:12O:16 )
查看答案和解析>>
科目: 来源: 题型:
【题目】酚酞的结构简式如图,下列关于酚酞的说法一定正确的是
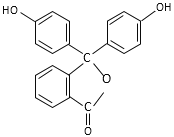
A. 酚酞的分子式是C20H12O4
B. 分子中的碳原子不在同一平面
C. 1 mol酚酞最多可消耗2 mol NaOH
D. 常温下,由水电离的c(H+)=10-13mol·L-1的溶液中滴入酚酞试液后,溶液呈红色
查看答案和解析>>
科目: 来源: 题型:
【题目】ClO2是一种国际公认的安全、无毒的绿色消毒剂,沸点11℃,凝固点-59℃。工业上,可用下列原理制备ClO2(液相反应):![]() 。设NA是阿伏伽德罗常数的值。下列说法正确的是( )
。设NA是阿伏伽德罗常数的值。下列说法正确的是( )
A.在标准状况下,2240mL ClO2含有原子数为0.3NA
B.若生成1.5mol Na2SO4,则反应后的溶液中Fe3+数目为0.2NA
C.48.0g FeS2完全反应,则上述反应中转移电子数为6NA
D.每消耗30mol NaClO3,生成的水中氢氧键数目为14NA
查看答案和解析>>
科目: 来源: 题型:
【题目】工业从废铅酸蓄电池的渣泥(主要成分为PbSO4、PbO2)回收铅。RSR 工艺的主要流程如下:
![]()
(1)铅酸蓄电池放电时总反应为:
Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(l)
正极反应:PbO2(s) + SO42-(aq) + 4H+(aq) + 2e- = PbSO4(s) + 2H2O(l)
负极反应:________。
(2)向渣泥中加入Na2CO3溶液将PbSO4转化为更难溶的PbCO3。
①用化学平衡移动原理解释其原因:________。
②工业上常用NaHCO3溶液代替Na2CO3溶液,将PbSO4转化为PbCO3。PbSO4与NaHCO3溶液或Na2CO3溶液不同物质的量比时,PbSO4的转化率见下表。
Ⅰ | n(PbSO4)∶ n(NaHCO3) | 1∶1.5 | 1∶2 | 1∶3 |
PbSO4转化率/% | 95.5 | 96.9 | 97.8 | |
Ⅱ | n(PbSO4)∶ n(Na2CO3) | 1∶1.5 | 1∶2 | 1∶3 |
PbSO4转化率/% | 98 | 98 | 98 |
依据上表数据,物质的量比相同时,Ⅱ中PbSO4的转化率比Ⅰ中的略大,原因是________。
③上述反应除生成PbCO3外,还可能生成碱式碳酸铅[2PbCO3·Pb(OH)2],二者受热都易分解生成PbO。通过实验确定产物中含有2PbCO3·Pb(OH)2,则该实验操作及现象是________;通过定量实验确定产物中2PbCO3·Pb(OH)2的含量,则需测定的数据是________。
(3)渣泥中加入Na2SO3溶液,利用其性质是________。
(4)H2SiF4溶液溶解PbCO3的化学方程式是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com