
科目: 来源: 题型:
【题目】铁是地壳中含量较丰富的元素,仅次于氧、硅、铝元素,其单质及合金是在生产生活中应用广泛的金属材料。化学上常用KSCN溶液等来检验溶液中是否存在Fe3+。
(1)Fe3+离子基态的电子排布式可表示为___。
(2)一种铁晶体的晶胞属于体心立方堆积,则该晶胞中所包括的铁原子的个数是___。
(3)C、N两种元素的简单气态氢化物的热稳定性由强到弱的顺序为___。(填化学式)
(4)C、N、O三种元素的第一电离能由大到小的顺序为___(填元素符号)。
(5)离子化合物Fe2O3的熔点高于KC1的熔点的原因是___。
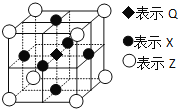
(6)据报道:由Q、X、Z三种元素形成的一种晶体具有超导性,其晶体结构如图所示。晶体中距每个X原子周围距离最近的Q的原子的个数是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液由弱酸(HR)及其盐(NaR)组成,浓度均为1 molL-1,25℃时向该溶液通入HCl气体或滴入NaOH溶液,溶液pH随加入的H+或OH-的物质的量发生变化的情况如图。下列说法不正确的是

A. A、B、C三点所表示的溶液中水的电离程度依次增大
B. 加入1 mol NaOH后,溶液中c(Na+)=c(R-)
C. 通入HCl, R-的水解程度增大,HR的电离常数减小
D. 未加HCl和NaOH时,溶液中c(R-)>c(Na+)>c(HR)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.图1表示相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线II为盐酸,且b点溶液的导电性比a点强
B.图1中,中和等体积的两种酸,消耗等浓度的NaOH溶液体积V(I)>V(II)
C.图2中纯水仅升高温度,就可以从a点变到c点
D.图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
查看答案和解析>>
科目: 来源: 题型:
【题目】对于2SO2(g)+O2(g) 2SO3(g),ΔH<0,根据下图,下列说法错误的是( )
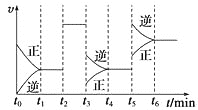
A.t2时使用了催化剂B.t3时采取减小反应体系压强的措施
C.t5时采取升温的措施D.反应在t6时刻,SO3体积分数最大
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A. A的转化率变大B. 平衡向正反应方向移动
C. D的体积分数变大D. a<c+d
查看答案和解析>>
科目: 来源: 题型:
【题目】一种测定水样中溴离子的浓度的实验步骤如下:
①向锥形瓶中加入处理后的水样25.00mL,加入几滴NH4Fe(SO4)2溶液。
②加入V1mL c1mol·L-1 AgNO3溶液(过量),充分摇匀。
③用c2mol·L-1KSCN标准溶液进行滴定,至终点时消耗标准溶液V2mL 。
(已知:Ksp(AgBr)=7.7×10-13,Ag++SCN-= AgSCN(白色)↓,Ksp(AgSCN)=1×10-12)下列说法不正确的是
A. 滴定终点时,溶液变为红色
B. 该滴定法需在碱性条件下进行
C. AgBr(s)+SCN-![]() AgSCN(s)+Br-(aq)的平衡常数K=0.77
AgSCN(s)+Br-(aq)的平衡常数K=0.77
D. 该水样中溴离子浓度为:c(Br-)=(c1V1-c2V2)/25.00mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中错误的是
A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构
B.1mol金刚石晶体中,平均含有2molC—C键
C.构成单质分子的微粒之间不一定存在共价键
D.某气态团簇分子结构如图所示,该分子的分子式为EF或FE
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,用0.1000mol·L-1的NaOH溶液分别滴定20.00mL均为0.1000mol·L-1的三种酸HX、HY、HZ ,滴定曲线如图所示。下列说法错误的是
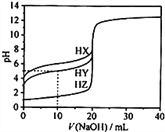
A. HZ是强酸,HX、HY是弱酸
B. 根据滴定曲线,可得Ka(HY)≈10-5
C. 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D. 将上述HY与HZ溶液等体积混合达到平衡时:C(H+)=c(OH-)+c(Z-)+c(Y-)
查看答案和解析>>
科目: 来源: 题型:
【题目】煤气化是有效利用化石能源的手段之一,有关反应为
①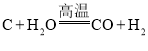 、②
、②![]() ,获得的气体称为水煤气。某研究性学习小组为探究气体的成分,进行了如下实验。
,获得的气体称为水煤气。某研究性学习小组为探究气体的成分,进行了如下实验。
(实验)使水蒸气通过灼热的焦炭,收集反应后流出的气体。
(提出假设)对气体的成分提出了三种假设。
假设1:该气体是![]() 、
、![]() 、
、![]() 。
。
假设2:该气体是![]() 、
、![]() 、
、![]() 。
。
(1)假设3:___________________________________________。
(设计实验方案,验证假设)
拟用图中提供的仪器,选择必要的试剂,设计一个实验,验证上述假设3。(加热装置和导管等在图中略去,实验前装置内部的空气已经排尽)


(2)按气流从左至右连接各仪器,用题中小写字母表示接口的连接顺序(仪器可重复使用):混合气→dc→______→______→______→______→______→ij。
(3)仪器A中需加入药品的名称是____________,其中反应的化学方程式可能有___________________________________________。
(4)仪器B中需加入药品的名称是______________,其作用是____________________________。
(思考与交流)
(5)本实验的尾气需要处理,处理的方法为_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A. 该反应的速率主要取决于①的快慢
B. NOBr2是该反应的催化剂
C. 正反应的活化能比逆反应的活化能小a kJ·mol-1
D. 增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com