
科目: 来源: 题型:
【题目】随着我国对环境问题的重视,碳、氮及其化合物的研究备受关注。
已知:Ⅰ![]()
![]() ;
;
Ⅱ![]()
![]() ;
;
Ⅲ![]()
![]()
![]() .
.
请回答下列问题:
(1)![]() ________。
________。
(2)一定温度下,向刚性容器中充入![]() 和足量
和足量![]() ,发生上述反应,部分物质的物质的量浓度随时间的变化情况如图所示。
,发生上述反应,部分物质的物质的量浓度随时间的变化情况如图所示。

![]() 已知曲线a代表
已知曲线a代表![]() 的浓度变化,曲线b代表NO的浓度变化,则曲线c代表________的浓度变化。
的浓度变化,曲线b代表NO的浓度变化,则曲线c代表________的浓度变化。
![]() 该刚性容器的容积为________;
该刚性容器的容积为________;![]() 内,
内,![]() 的消耗速率
的消耗速率![]() ________。
________。
![]() 该条件下,反应Ⅰ和反应Ⅱ中活化能较大的是________
该条件下,反应Ⅰ和反应Ⅱ中活化能较大的是________![]() 填“反应Ⅰ”或“反应Ⅱ”
填“反应Ⅰ”或“反应Ⅱ”![]() ,原因为________。
,原因为________。
![]() 该温度下,反应Ⅲ的化学平衡常数
该温度下,反应Ⅲ的化学平衡常数![]() Ⅲ
Ⅲ![]() ________。
________。
(3)若其他条件不变,将恒温容器改为绝热容器,再次达到平衡后,与原平衡相比,CO的体积分数________![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]() ,原因为________。
,原因为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组为探究铁发生电化学腐蚀的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图甲)从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化结果如图,下列叙述错误的是( )
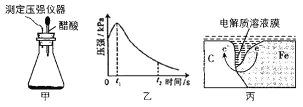
A.图丙中,发生腐蚀时电子转移方向如箭头所示
B.图乙中,t2时容器中压强明显小于起始压强是因为铁粉发生了吸氧腐蚀
C.碳粉表面的电极反应式只有:O2+4e-+2H2O=4OH-
D.若将丙图中的C 换成Zn,铁的腐蚀速率会大大降低,这是是利用了牺牲阳极的阴极保护法
查看答案和解析>>
科目: 来源: 题型:
【题目】下列变化中,气体被还原的是
A.水蒸气使 CuSO4固体变蓝B.氯气使浅绿色 FeC12 溶液变黄
C.H2使灼热CuO 固体变红D.氨气使A1Cl3溶液产生白色沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】多晶硅是广泛用于制造半导体收音机、录音机、电冰箱、彩电、录像机、电子计算机等的基础材料。以下是由石英砂制备多晶硅的简易过程。
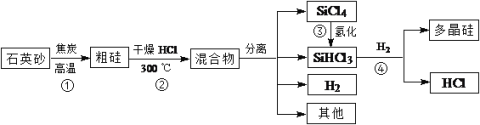
回答下列问题:
(1)反应①中氧化剂与还原剂的物质的量之比为_______。反应②中生成SiHCl3的化学方程式为___________。分离混合物采用的方法为蒸馏,其原理是利用了物质的______不同。
(2)反应③氢化过程中所需的高纯度H2可通过电解精制的饱和食盐水制得,电解过程中同时生成一种黄绿色的气体和一种易溶、易电离的碱,电解反应的离子方程式是________。粗盐水精制过程中,为有效除去Ca2+、Mg2+、SO42-等杂质,要按__________顺序(填标号)加入下列溶液:a.NaOH b.Na2CO3 c.BaCl2,过滤后再向滤液中加________调节pH。
(3)反应④中H2还原SiHCl3过程中若混入O2,除可能引起爆炸外,还可能引起_____。由粗硅制备多晶硅的过程中,循环使用的物质除SiCl4、SiHCl3和Si外,还有__________(填分子式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】高炉炼铁中发生的反应为:FeO(s)+CO(g)![]() Fe(s)+CO2(g) △H>0。已知t℃时,平衡常数K=0.25。
Fe(s)+CO2(g) △H>0。已知t℃时,平衡常数K=0.25。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数K_____(填“增大”、“减小”或“不变”,下同),高炉内CO2和CO的体积比____
(2)t℃时测得高炉中c(CO2)=0.020 mol·Lˉ1,c(CO)=0.1 mol·Lˉ1,在这种情况下,该反应是否处于化学平衡状态_______(填“是”或“否”),此时,化学反应速率是υ(正)_____υ(逆)(填“大于”、“小于”或“等于”),其原因是________________
(3)若在1L密闭容器中加入0.02mol FeO(s),并通入x mol CO,t℃时反应达到平衡。此时FeO(s)的转化率为50%,则x=_______________。
(4)如图为t2时刻后改变条件平衡体系中化学反应速率随时间变化的情况,且四个阶段各改变一种条件并且改变的条件均不同。已知,t3~t4阶段为使用催化剂,则t4时刻改变的条件为_____________,t5时刻改变的条件为____________

查看答案和解析>>
科目: 来源: 题型:
【题目】分子式为C12H14O2的F有机物广泛用于香精的调香剂。为了合成该物质,某实验室的科技人员设计了下列合成路线:
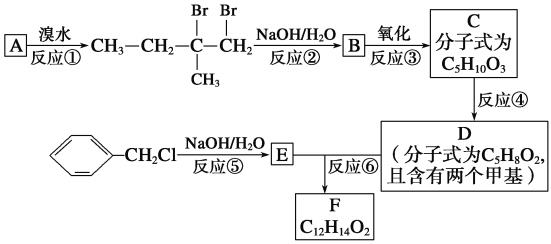
试回答下列问题:
(1)A物质在核磁共振氢谱中能呈现________种峰;峰面积比为__________。
(2)上述合成路线中属于取代反应的是__________(填编号)。
(3)写出反应⑤、⑥的化学方程式:
⑤____________________________________________________________________;
⑥____________________________________________________________________。
(4)F有多种同分异构体,请写出符合下列条件的所有物质结构简式:①属于芳香族化合物,且含有与F相同的官能团;②苯环上有两个取代基,且苯环上的一氯代物只有两种;③其中一个取代基为—CH2COOCH3:______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁均为中学化学常见的物质,它们之间的转化关系如图(反应条件及其它产物已略去).下列说法不正确的是( )
![]()
A. 若甲是AlCl3溶液,则丁可能是NaOH溶液
B. 若甲是Fe,则丁可能是Cl2
C. 若丁是CO2,则甲可能为Mg
D. 若丁是O2,则乙、丙的相对分子质量可能相差16
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭容器中充入2molA和1molB发生反应:2A(g)+B(g)![]() xC(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol,B:0.3mol,C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%。则x的值为( )
xC(g),达到平衡后,C的体积分数为W%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol,B:0.3mol,C:1.4mol充入容器,达到平衡后,C的体积分数仍为W%。则x的值为( )
A.只能为2B.只能为3C.只能为4D.可能为2或3
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E 五种元素的原子序数依次增大,B、C 的阳离子与A的阴离子和氖原子的电子层结构相同;A、B可形成离子化合物B2A;C的氧化物既能与强酸反应,又能与强碱反应;D的原子结构示意图为: ;E的最外层电子数是电子层数的2倍。试回答下列各问题:
;E的最外层电子数是电子层数的2倍。试回答下列各问题:
(1)B、D元素分别为_________、_________;
(2)D元素位于元素周期表中第_______周期、第______族;
(3)化合物B2A的电子式____________________;
(4)E的最高价氧化物的水化物的分子式是________________________。
(5)D与NaOH溶液反应的化学方程式:_______________________________。
(6)C的氧化物与E的最高价氧化物的水化物溶液反应的离子方程式: ________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com