
科目: 来源: 题型:
【题目】氰化物有剧毒,冶金工业会产生大量含氰化物的废水,其中氰化物以CN-等形式存在于废水中。某化学小组同学对含氰化物废水处理进行研究。
Ⅰ.查阅资料:含氰化物的废水处理方法。
利用强氧化剂将氰化物氧化为无毒物质,如以TiO2为催化剂用NaClO将CN-氧化成CNO-(CN-和CNO-中N元素均为-3价),CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。
Ⅱ.实验验证:处理CN-的效果。
化学兴趣小组的同学在密闭系统中用如图装置进行实验,以测定CN-被处理的百分率,实验步骤如下:

步骤1:取一定量废水进行加热蒸发、浓缩。
步骤2:取浓缩后含CN-的废水与过量NaClO溶液的混合液共200 mL(设其中CN-的浓度为0.2 mol·L-1)倒入甲中,塞上橡皮塞。
步骤3:点燃酒精灯对丁装置加热。
步骤4:打开甲上的橡皮塞和活塞,使甲中溶液全部放入乙中,关闭活塞。
步骤5:打开活塞K,通一段时间N2,关闭活塞K。
步骤6:实验完成后测定干燥管Ⅰ(含碱石灰)的质量m2[实验前干燥管Ⅰ(含碱石灰)的质量m1]。
回答下列问题:
(1)在处理方法中,在酸性条件下NaClO和CNO-反应的离子方程式为:___________。
(2)对丁装置加热放在步骤3进行的原因是:___________。
(3)丙装置中的试剂是:___________。
(4)装置中石棉绒作用为:___________。
(5)干燥管Ⅱ的作用是:_____________________________。
(6)请简要说明实验中通入N2的目的是:______________________________。
(7)若干燥管Ⅰ中碱石灰增重1.408 g,则该实验中测得CN-被处理的百分率为:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,容积为2L的密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示。
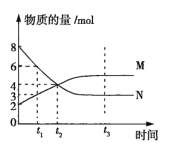
(1)该反应的化学方程式为___。
(2)比较t2、t3时正、逆反应速率的大小(用v正、v逆表示):t2时__;t3时__。
(3)若t2=2min,则反应开始至t2时,M的平均反应速率为__。
(4)下列说法可以表明该反应已达到平衡状态的是__(填序号)。
A.混合气体的密度不变
B.正、逆反应速率都等于零
C.M、N的物质的量浓度不变
D.M、N的物质的量浓度相等
(5)t3时化学反应达到平衡状态,请写出3个可以提高此时该反应化学反应速率的方法:__。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以铝铁质岩![]() 主要成分是
主要成分是![]() 、
、![]() 和
和![]() 为原料制备
为原料制备![]() 和粗硅,其流程如图所示:
和粗硅,其流程如图所示:
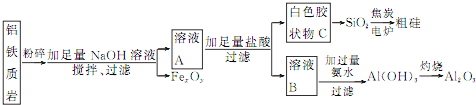
![]() 制备粗硅的化学方程式为 ______ 。
制备粗硅的化学方程式为 ______ 。
![]() 溶液B中加氨水生成
溶液B中加氨水生成![]() 的离子方程式为 ______,在空气中灼烧固体
的离子方程式为 ______,在空气中灼烧固体![]() 时,用到多种硅酸盐质仪器,除玻璃棒、酒精灯、泥三角外,还有 ______
时,用到多种硅酸盐质仪器,除玻璃棒、酒精灯、泥三角外,还有 ______ ![]() 填仪器名称
填仪器名称![]() 。
。
![]() 在高温下,氧化铝可以与氮气、碳反应,生成一种耐高温、抗冲击的氮化铝和一种有毒气体,该反应的化学方程式为 ______ ;该反应中每生成2mol氮化铝,
在高温下,氧化铝可以与氮气、碳反应,生成一种耐高温、抗冲击的氮化铝和一种有毒气体,该反应的化学方程式为 ______ ;该反应中每生成2mol氮化铝,![]() 得到电子的物质的量为 ______ mol。
得到电子的物质的量为 ______ mol。
![]() 某实验小组用CO还原法定量测定
某实验小组用CO还原法定量测定![]() 的组成,称取mg样品进行定量测定。
的组成,称取mg样品进行定量测定。
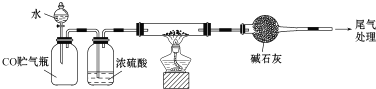
![]() 根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品, ______
根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品, ______ ![]() 请按正确顺序填入下列步骤的标号
请按正确顺序填入下列步骤的标号![]() 。
。
![]() 点燃酒精灯
点燃酒精灯![]() 打开分液漏斗活塞
打开分液漏斗活塞![]() 停止加热,充分冷却
停止加热,充分冷却 ![]() 关闭分液漏斗活塞
关闭分液漏斗活塞![]() 收集气体并检验纯度
收集气体并检验纯度
![]() 若实验中每步反应都进行完全,反应后样品质量减少了ng,则
若实验中每步反应都进行完全,反应后样品质量减少了ng,则![]() 中x:
中x:![]() ______
______ ![]() 若实验中
若实验中![]() 未被充分还原,则x:y的值 ______
未被充分还原,则x:y的值 ______ ![]() 填“偏大”“偏小”或“无影响”
填“偏大”“偏小”或“无影响”![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知草酸为二元中强酸,具有较强还原性,且![]() ,下列说法正确的是
,下列说法正确的是![]()
A.草酸与氢氧化钠溶液混合呈中性时,溶液中存在:![]()
B.![]() 与NaClO溶液混合,反应的离子方程式为:
与NaClO溶液混合,反应的离子方程式为:![]()
C.![]() 溶液中:
溶液中:![]()
![]()
![]()
![]()
D.草酸使酸性![]() 溶液褪色,离子方程式为:
溶液褪色,离子方程式为:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温恒容下,将2mol气体A和2mol气体B通体积为2L的密闭容器中,发生如下反应:2A(g)+B(g)![]() xC(g)+2D(s),2min后反应达到平衡态,此时剩余1.2molB,并测得C的浓为1.2mol·L-1。
xC(g)+2D(s),2min后反应达到平衡态,此时剩余1.2molB,并测得C的浓为1.2mol·L-1。
(1)从反应开始至达到平衡状态,生成C的平均应速率为_。
(2)x=__。
(3)下列各项可作为该反应达到平衡状态标志是_(填序号)。
A.压强不再变化
B.气体密度不再变化
C.气体的平均相对分子质量不再变化
D.A的消耗速率与B的消耗速率之比为
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯![]() 作为一种高效强氧化剂,已被联合国世界卫生组织
作为一种高效强氧化剂,已被联合国世界卫生组织![]() 列为AⅠ级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中
列为AⅠ级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中![]() 的质量分数高于
的质量分数高于![]() 等均有可能引起爆炸,易与碱液反应生成盐和水。
等均有可能引起爆炸,易与碱液反应生成盐和水。
![]() 某研究小组设计如图所示实验制备
某研究小组设计如图所示实验制备![]() 溶液,其反应的化学方程式为
溶液,其反应的化学方程式为![]() 。
。

![]() 在反应开始之前将烧杯中的水加热到
在反应开始之前将烧杯中的水加热到![]() ,然后停止加热,并使其温度保持在
,然后停止加热,并使其温度保持在![]() 之间。控制温度的目的是___________,图中装置中缺少的一种必需的玻璃仪器是_______________________。
之间。控制温度的目的是___________,图中装置中缺少的一种必需的玻璃仪器是_______________________。
![]() 装置A用于溶解产生的二氧化氯气体,其中最好盛放________
装置A用于溶解产生的二氧化氯气体,其中最好盛放________![]() 填标号
填标号![]() 。
。
a.20mL60℃的温水 b.100mL冰水 c.100mL饱和食盐水 d.100mL沸水
![]() 在烧瓶中加入12.25gKClO3和9g草酸
在烧瓶中加入12.25gKClO3和9g草酸![]() ,然后再加入足量的稀硫酸,水浴加热,反应后生成
,然后再加入足量的稀硫酸,水浴加热,反应后生成![]() 的质量为________。
的质量为________。
![]() 用
用![]() 处理过的饮用水
处理过的饮用水![]() 为
为![]() 常含有一定量对人体不利的亚氯酸根离子
常含有一定量对人体不利的亚氯酸根离子![]() 。饮用水中
。饮用水中![]() 、
、![]() 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至![]() ;
;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的![]() 溶液滴定至终点;
溶液滴定至终点;
步骤5:再调节溶液的![]() ;
;
步骤6:继续用相同浓度的![]() 溶液滴定至终点。
溶液滴定至终点。
![]() 步骤1中若要量取20.00mL水样,则应选用的仪器是____________________。
步骤1中若要量取20.00mL水样,则应选用的仪器是____________________。
![]() 步骤
步骤![]() 的目的是测定水样中
的目的是测定水样中![]() 的含量,其反应的化学方程式为2ClO2+2KI=2KClO2+I2,2Na2S2O3+I2=Na2S4O6+2NaI,则步骤4中加入的指示剂为______________,滴定达到终点时溶液的颜色变化为______________。
的含量,其反应的化学方程式为2ClO2+2KI=2KClO2+I2,2Na2S2O3+I2=Na2S4O6+2NaI,则步骤4中加入的指示剂为______________,滴定达到终点时溶液的颜色变化为______________。
![]() 步骤5的目的是使
步骤5的目的是使![]() 将溶液中的
将溶液中的![]() 还原为
还原为![]() 以测定其含量,该反应的离子方程式为____________________________。
以测定其含量,该反应的离子方程式为____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于有机物 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )
A. 它的系统名称是2,4-二甲基-4-戊烯
B. 它的分子中至少有5个碳原子在同一平面上
C. 它与甲基环己烷(![]() )互为同分异构体
)互为同分异构体
D. 该有机物与氢气完全加成后的产物的一氯取代产物共有4种
查看答案和解析>>
科目: 来源: 题型:
【题目】用![]() 表示阿伏加德罗常数的值,下列叙述正确的是( )
表示阿伏加德罗常数的值,下列叙述正确的是( )
A.![]() 个
个![]() 胶体粒子的质量为78g
胶体粒子的质量为78g
B.![]() g
g![]() 和CuO的混合物中含有铜原子数为
和CuO的混合物中含有铜原子数为![]()
C.在![]() 的碳酸钠溶液中,阴离子总数一定大于
的碳酸钠溶液中,阴离子总数一定大于![]()
D.标准状况下,![]() L己烷中共价键数目为
L己烷中共价键数目为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】葡萄糖酸亚铁((C6H11O7)2Fe)是常用的补铁剂,易溶于水,几乎不溶于乙醇。用下图装置制备FeCO3,并利用FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:

(1)a的名称为_________。
(2)打开a中K1、K3,关闭K2,一段时间后,关闭K3,打开K2。在_________(填仪器标号)中制得碳酸亚铁。实验过程中产生的H2作用有_________、____________。(写2条)
(3)将制得的碳酸亚铁浊液过滤、洗涤。如过滤时间过长会发现产品部分变为红褐色。用化学方程式说明原因____________。
(4)将葡萄糖酸与碳酸亚铁混合,加入乙醇、过滤、洗涤、干燥。加入乙醇的目的是_________________。
(5)用 NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时有气体产生,离子方程式为______________,此法产品纯度更高,原因是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是( )
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是( )
A. 容器内的总压强不随时间变化
B. 断裂4molH—O键的同时,断裂2molH—H键
C. 混合气体分子的总数不变
D. 反应不再进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com