含镁3%-5%的镁铝合金,现已成为轮船制造、化工生产、机械制造等行业的重要原材料.现有一块已知质量为m
1g的镁铝合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:
镁铝合金
溶液
得到沉淀的质量为m
2g;
实验设计2:
镁铝合金
生成的气体在标准状况下的体积为V
1L.
实验设计3:
镁铝合金
生成的气体在标准状况下的体积为V
2L.
请回答以下问题:
(1)写出实验设计1中单质铝发生反应的离子方程式:
2Al+6H+═2Al3++3H2↑?、Al3++4OH-═[Al(OH)4]-或Al3++3OH-═Al(OH)3↓?Al(OH)3+OH-═[Al(OH)4]-?
2Al+6H+═2Al3++3H2↑?、Al3++4OH-═[Al(OH)4]-或Al3++3OH-═Al(OH)3↓?Al(OH)3+OH-═[Al(OH)4]-?
(2)写出实验设计2中反应的离子方程式:
2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑
2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑
(3)判断这几种实验设计能否求出镁的质量分数,能求出的用题目提供的数据将镁的质量分数表示出来,不能求出的就空着不填.
①实验设计1
②实验设计2
③实验设计3
.

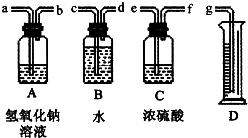 某环保部门调查指出:大气中的酸性气体有相当一部分来自全国数以万计的高校、中学的化学实验室.为此某校化学研究小组的同学拟从下面提供的实验用品中选取合适的装置和药品,组装成一套实验装置,用来粗略测定实验室里空气中全部酸性气体的体积分数.
某环保部门调查指出:大气中的酸性气体有相当一部分来自全国数以万计的高校、中学的化学实验室.为此某校化学研究小组的同学拟从下面提供的实验用品中选取合适的装置和药品,组装成一套实验装置,用来粗略测定实验室里空气中全部酸性气体的体积分数.