
科目: 来源: 题型:
【题目】下列说法正确的是![]()
A.![]() 有机物
有机物![]() 的分子结构中含有的
的分子结构中含有的![]() 键数目一定为
键数目一定为![]()
B.一定温度下,氯化铵水解离子方程式:![]() ,若用
,若用![]() 表示的离子积,
表示的离子积,![]() 表示氨水电离常数,则氯化铵水解平衡常数
表示氨水电离常数,则氯化铵水解平衡常数![]()
C.已知反应:![]() :
:![]() :
:![]() ;则在酸性溶液中氧化性:
;则在酸性溶液中氧化性:![]()
D.已知
共价键 |
|
|
|
|
键能 | 360 | 436 | 431 | 176 |
则反应![]() 的焓变为:
的焓变为:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺如下:

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有___________、__________。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:___________。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | —— | —— | —— |
沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有___________;但溶液的pH不能超过8,其理由是_____________________。
(4)钠离子交换树脂的反应原理为:Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在某温度时,将n![]() 氨水滴入10mL
氨水滴入10mL![]() 盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是
盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是![]()
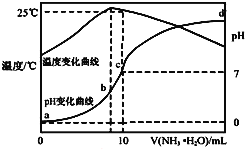
A.a点![]()
B.水的电离程度:![]()
C.b点:![]()
D.![]() 时
时![]() 水解常数为
水解常数为![]()
![]() 用n表示
用n表示![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H3PO4是一种三元中强酸。25℃时,某浓度H3PO4溶液中逐滴加入NaOH溶液,滴加过程中各种含磷微粒的物质的量分数δ随溶液pH的变化曲线如下图所示。下列说法正确的是

A. 曲线2和曲线4分别表示δ(HPO42-)和δ(PO43-)变化
B. 25℃时,H3PO4的电离常数K1:K2=105.1
C. pH=7.2时,溶液中由水电离出的c(H+)=10-7.2mol/L
D. pH=12.3时,溶液中2c(Na+)=5c(H2PO4-)+5c(HPO42-)+5c(PO43-)+5c(H3PO4)
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将amol氮气与bmol氢气的混合气体通入一个固定容积的密闭容器中,发生反应N2(g)+3H2(g) ![]() 2NH3(g)。
2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,则a值为________。
(2)反应达到平衡时,混合气体的体积为716.8 L(标准状况下),其中氨气体积分数为25%,平衡时氨气的物质的量为________。
(3)原混合气体与平衡混合气体的总物质的量之比(写最简整数比,下同)n始∶n平=______。
(4)原气体中a∶b=________。
(5)达到平衡时混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是( )
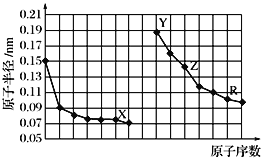
A. Z和R所形成的化合物,不能通过溶液中复分解反应而制得
B. 简单离子的半径关系是:R>Y>Z>X
C. X和Y所形成的一种化合物,可用于自来水消毒
D. 工业上获得单质Z的方法,一般是通过电解其熔融氯化物来实现
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.某有机物燃烧只生成![]() 和
和![]() ,且二者物质的量相等,则此有机物的组成为
,且二者物质的量相等,则此有机物的组成为![]()
B.—定压强下, ![]() 气态烃在足量的氧气中燃烧,将产生的气体通过浓硫酸后气体体积为
气态烃在足量的氧气中燃烧,将产生的气体通过浓硫酸后气体体积为![]() ,则生成的水蒸气的体积为
,则生成的水蒸气的体积为![]()
C.相同质量的烃,完全燃烧,消耗![]() 越多,烃中含氢量越高
越多,烃中含氢量越高
D.某气态烃![]() 与足量
与足量![]() 恰好完全反应,如果反应前后气体体积不变(温度大于100℃),则
恰好完全反应,如果反应前后气体体积不变(温度大于100℃),则![]() ;若体积减小,则
;若体积减小,则![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是( )
A.用来制造电线电缆的聚乙烯树脂属于热塑性高分子材料
B.研发可降解高分子材料,可以减少“白色污染”
C.棉、麻、羊毛及合成纤维完全燃烧都只生成![]() 和
和![]()
D.硅橡胶![]() 可由
可由![]() 经水解、缩聚两步反应制得
经水解、缩聚两步反应制得
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:在![]() 时,
时,![]()
![]()
![]()
![]()
![]() 、
、![]() 、
、![]()
又已知:![]() ,下列说法正确的是
,下列说法正确的是![]()
A.醋酸钠水解的平衡常数![]() 随温度升高而减小
随温度升高而减小
B.![]() 醋酸钠溶液pH为m,其水解的程度
醋酸钠溶液pH为m,其水解的程度![]() 已水解的醋酸钠与原有醋酸钠的比值
已水解的醋酸钠与原有醋酸钠的比值![]() 为a;
为a;![]() 醋酸钠溶液pH为n,水解的程度为b,则
醋酸钠溶液pH为n,水解的程度为b,则![]() 、
、![]()
C.醋酸钠的水解的平衡常数![]()
D.在某溶液中含![]() 、
、![]() 、
、![]() 三种离子的浓度均为
三种离子的浓度均为![]() ,向其中加入固体醋酸钠,使其浓度为
,向其中加入固体醋酸钠,使其浓度为![]() ,以上三种金属离子中只有
,以上三种金属离子中只有![]() 能生成沉淀
能生成沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
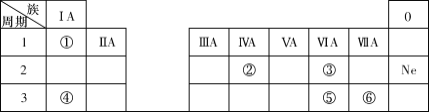
(1)②的元素符号是__________;该元素的最高价氧化物的电子式为__________;
(2)⑤和⑥两种元素的非金属性强弱关系是:⑤________⑥(填“>”或“<”);
(3)①和③两种元素组成的化合物中含有的化学键为__________(填“离子键”或“共价键”)
(4)④和⑥两种元素组成的化合物与AgNO3溶液反应的离子方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com