
科目: 来源: 题型:
【题目】在某温度时,将n mol·L-1氨水滴入10 mL 1.0 mol·L-1 盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是

A. a点KW=1.0×10-14
B. b点:c(NH)>c(Cl-)>c(H+)>c(OH-)
C. 25 ℃时,NH4Cl水解常数为(n-1)×10-7(用n表示)
D. d点水的电离程度最大
查看答案和解析>>
科目: 来源: 题型:
【题目】对于溶液的酸碱性说法正确的是
A.含OH-的溶液一定呈碱性B.在100°C时,纯水的pH<7,因此显酸性
C.c(H+)=c(OH-)的溶液一定呈中性D.pH=14的溶液碱性最强
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某二元酸(化学式用H2A表示)在水中的电离方程式是H2A═H++HA-,HA-![]() H++A2-;试完成下列问题:
H++A2-;试完成下列问题:
NaHA溶液显__(填“酸性”、“中性”或“碱性”),Na2A溶液显__(填“酸性”、“中性”或“碱性”)。理由是__(用离子方程式表示)。
(2)pH=5的NH4Cl溶液与pH=5的HCl溶液中由水电离出的c(H+)分别是__、__。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚氯酸钠![]() 用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成
用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成![]() 、
、![]() 、
、![]() 、
、![]() 等,其中
等,其中![]() 和
和![]() 都具有漂白作用.已知
都具有漂白作用.已知![]() ,经测定
,经测定![]() 时各组分含量随pOH变化情况如图所示
时各组分含量随pOH变化情况如图所示![]() 没有画出
没有画出![]() ,此温度下,下列分析正确的是
,此温度下,下列分析正确的是![]()
![]()

A.![]() 的电离平衡常数的数值
的电离平衡常数的数值![]()
B.亚氯酸钠在酸性条件下较稳定
C.![]() 时,溶液中含氯微粒的浓度大小为:
时,溶液中含氯微粒的浓度大小为:![]()
D.同浓度的![]() 溶液和
溶液和![]() 溶液等体积混合,则混合溶液中有
溶液等体积混合,则混合溶液中有![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,XOH、YOH及ZOH三种一元碱的物质的量浓度均为0.100 mol·L-1,体积均为10.00 mL,分别用0.100 mol·L-1的HCl溶液滴定,滴定曲线如图所示。下列说法正确的是
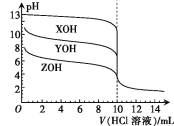
A.均可用酚酞作指示剂
B.电离平衡常数:Kb(YOH)<Kb(ZOH)
C.均滴入10.00 mL HCl溶液时,ZCl溶液中的水解程度最大
D.pH=11的YOH与pH=3的HCl溶液等体积混合:c(Cl-)>c(Y+)>c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示:横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-物质的量浓度的对数,回答下列问题。

(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为___。
(2)从图中数据计算可得Zn(OH)2的溶度积Ksp=___。
(3)某废液中含Zn2+,为提取Zn2+可以控制溶液pH的范围是___。
(4)泡沫灭火器内装有NaHCO3饱和溶液;灭火器内另有一容器中装有Al2(SO4) 3溶液,该溶液呈酸性的原因是:___(用离子方程式表示)。当意外失火时,使泡沫灭火器倒过来即可使药液混合,喷出CO2和Al(OH)3,阻止火势蔓延。其相关化学反应的离子方程式为:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是( )
A.用惰性电极电解熔融氯化钠:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-=Mn2++Cl2↑+2H2O
C.向Na[Al(OH)4]溶液中通入过量CO2制Al(OH)3:[Al(OH)4]-+CO2=Al(OH)3↓+HCO3-
D.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】已知299 K时,合成氨反应 N2(g ) + 3H2 ( g )![]() 2NH3( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
2NH3( g ) △H = -92.0 kJ/mol,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)
A. 一定大于92.0 kJB. 一定等于92.0 kJ
C. 一定小于92.0 kJD. 不能确定
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,用![]() 溶液分别滴定
溶液分别滴定![]() 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是
的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是![]()
![]()

A.Ⅱ表示的是滴定醋酸的曲线
B.![]() 时,滴定醋酸消耗的
时,滴定醋酸消耗的![]() 小于
小于![]()
C.![]() 时,两份溶液中
时,两份溶液中![]()
D.![]() 时,醋酸溶液中
时,醋酸溶液中![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,![]() 甲基
甲基![]() 中含有的中子数为
中含有的中子数为![]()
B.将![]() 溶于稀氨水中,所得溶液呈中性,则溶液中
溶于稀氨水中,所得溶液呈中性,则溶液中![]() 的数目为
的数目为![]()
C.![]() 和
和![]() 在催化剂和加热条件下充分反应生成NO的分子数为
在催化剂和加热条件下充分反应生成NO的分子数为![]()
D.常温下,![]() 的
的![]() 溶液中,发生电离的水分子数为
溶液中,发生电离的水分子数为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com