
科目: 来源: 题型:
【题目】下列表述正确的是
A. 苯和氯气生成C6H6Cl6的反应是取代反应
B. 乙烯与溴水发生加成反应的产物是CH2CH2Br2
C. 等物质的量的甲烷与氯气反应的产物是CH3Cl
D. 硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知SO2(g)+ 1/2 O2(g) ![]() SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为_________________。
SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为_________________。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_____________________________
(3)在一定条件下,CH4 和CO的燃烧的热化学方程式分别为:
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) △H = -890 kJ/mol
2CO ( g ) + O2 ( g ) = 2CO2 ( g ) △H = -566 kJ/mol
一定量的CH4和CO的混合气体完全燃烧时,放出的热量为262.9 kJ,生成的CO2用过量的饱和石灰水完全吸收,可得到50 g白色沉淀。求混合气体中CH4 和CO的体积比_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法中正确的是( )
A.下列各项(①温度;②浓度;③容量;④刻度;⑤刻度线),其中容量瓶上标有①③④
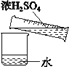
B.用18.4 mol/L的硫酸配制1 mol/L稀硫酸的实验有如图所示的操作
C.容量瓶用蒸馏水洗净后要烘干以除去残留的水
D.若用含有Na2O的NaOH配制溶液,则所配溶液浓度偏大
查看答案和解析>>
科目: 来源: 题型:
【题目】现有反应mA(g)+nB(g) ![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)若加入B(容器体积不变),则A的转化率______(填增大、减小或不变,下同),B的转化率______。
(2)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将______(填增大、减小或不变)。
(3)若B是有色物质,A、C均无色,则加入C(容积不变)时混合物颜色________(填变深、变浅或不变,下同),而维持容器内压强不变,充入Ne时,混合物的颜色_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) ![]() 2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300 ℃时,该反应的平衡常数表达式为:K =__________。已知K300 ℃<K350 ℃,则ΔH______0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率______(填“增大”“减小”或“不变” ) ,原因是 _______。
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时加入C、D各![]() mol。欲使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B_________mol。
mol。欲使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B_________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】砷As是第四周期ⅤA族元素,可以形成 As2S3、As2O5、H3AsO3、H3AsO4等 化合物,有着广泛的用途回答下列问题:
(1)写出砷的原子序数______________
(2)工业上常将含砷废渣主要成分为As2S3制成浆状,通入O2氧化,生成H3AsO4和单质硫,写出发生反应的化学方程式___________;该反应需要在加压下进行,原因是___________.
(3)已知:As(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s)△H1
H2(g)+2O2(g)=H3AsO4(s)△H1
H2(g)+![]() O2(g)=H2O(l)△H2
O2(g)=H2O(l)△H2
2As(s)+![]() O2(g)=As2O5(s)△H3
O2(g)=As2O5(s)△H3
则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的△H =___________
(4)298K时,将20mL 3x molL-1 Na3AsO3、20mL 3x molL-1 I2和20mL NaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是 ______ 填标号.
a .溶液的pH不再变化 b. v(I-)=2v(AsO33-)
c .c (AsO43-)/c (AsO33-)不再变化 d. c(I-)=ymolL-1
②tm时v正_____v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v正(填“大于”“小于”或“等于”)理由是 _____
④若平衡时溶液c(OH-)=1 mol/L,则该反应的平衡常数K为 ______________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关从海带中提取碘的实验原理和装置能达到实验目的的是

A. 用装置甲灼烧碎海带
B. 用装置乙过滤海带灰的浸泡液
C. 用装置丙制备用于氧化浸泡液中I的Cl2
D. 用装置丁吸收氧化浸泡液中I后的Cl2尾气
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示装置,室温下密闭容器内分别充入空气和H2.O2的混合气体在可移动的活塞两边,在标准状况下若将H2.O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2.O2的体积比最接近于 ( )

①2:7 ②5:4 ③4:5 ④7:2
A.①②B.②④C.③④D.①③
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:

(1)该反应的化学方程式为___________________________。
(2)反应开始至2min,以气体Z表示的平均反应速率为______________。
(3)平衡时X的转化率为_____________ 。
(4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:①此时体系内压强与开始时压强之比为________________;②达平衡时,容器内混合气体的平均相对分子质量比起始投料时____________________(填“增大”“减小”或“相等”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com