
科目: 来源: 题型:
【题目】氨为重要化工原料,有广泛用途。
(1)合成氨中的氢气可由下列反应制取:
a.CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H=+216.4KJ/mol
CO(g)+3H2(g) △H=+216.4KJ/mol
b.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.2kJ/mol
CO2(g)+H2(g) △H=-41.2kJ/mol
则反应CH4(g)+2H2O(g)![]() CO2(g)+4H2(g) △H=______。
CO2(g)+4H2(g) △H=______。
(2)起始时投入氮气和氢气分别为1mol、3mol,在不同温度和压强下合成氨。平衡时混合物中氨的体积分数与温度关系如图。

①恒压时,反应一定达到平衡状态的标志是______(填序号):
A.N2和H2的转化率相等 B.反应体系密度保持不变
C.![]() 的比值为3:2 D.
的比值为3:2 D.![]() =2
=2
②P1______P2(填“>”、“<”、“=”,下同):反应平衡常数:B点______D点;
③C点H2的转化率______;(数值保留0.1%)在A、B两点条件下,该反应从开始到平衡时生成氢气平均速率:v(A)______v(B)(填“>”、“<”、“=”)。
(3)已知25℃时由Na2SO3和NaHSO3形成的混合溶液恰好呈中性,则该混合溶液中各离子浓度的大小顺序为______________(已知25℃时,H2SO3的电离平衡常数Ka1=1×10-2,Ka2=1×10-7)
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室模拟工业利用氟磷灰石[Ca5(PO4)3F]生产磷铵[(NH4)3PO4]和白磷。其工艺流程如下图所示:

(1)氟磷灰石中磷元素的化合价为________,气体A 的电子式为________________;固体B 的化学式为____________________________。
(2)沸腾槽不能用陶瓷材质的原因是_______________________(用化学方程式表示)。
(3)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500 ℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为____________________________。
(4)在装置I中通入过量氨气的目的是___________________________________________。
(5)磷铵与草木灰不能混合使用的原因是______________________________________。
(6) (NH4)3PO4溶液中含磷离子浓度的大小顺序是_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)甲醇![]() 是重要的溶剂和替代燃料,工业上用CO和
是重要的溶剂和替代燃料,工业上用CO和![]() 在一定条件下制备
在一定条件下制备![]() 的反应为:
的反应为:![]() ,在体积为1L的恒容密闭容器中,充入
,在体积为1L的恒容密闭容器中,充入![]() 和
和![]() ,一定条件下发生上述反应,测得
,一定条件下发生上述反应,测得![]() 和
和![]() 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。

①从反应开始至达到平衡,用氢气表示的平均反应速率![]() ______
______![]() 。
。
②下列说法正确的是______![]() 填字母序号
填字母序号![]() 。
。
A.达到平衡时,CO的转化率为![]()
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前![]() 正
正![]() 逆
逆![]() ,2min后
,2min后![]() 正
正![]() 逆
逆![]()
③该条件下反应的平衡常数![]() ______。
______。
(2)已知:Ⅰ![]() 的燃烧热为
的燃烧热为![]()
Ⅱ![]()
![]()
![]()
Ⅲ.![]()
![]()
则①![]() ______。
______。
②对于可逆反应![]() 采取以下措施可以提高
采取以下措施可以提高![]() 产率的是______
产率的是______![]() 填字母
填字母![]()
A.降低体系的温度B.压缩容器的体积
C.减少水量D.选用适当的催化剂
(3)比亚迪双模电动汽车使用高铁电池供电。高铁电池的总反应为:![]() ,则充电时的阳极反应式为______。
,则充电时的阳极反应式为______。
(4)若往![]() 的弱酸
的弱酸![]() 溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如下图所示,下列有关说法正确的是______
溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如下图所示,下列有关说法正确的是______![]() 填序号
填序号![]() 。
。

①该烧碱溶液的浓度为0.02mol/L
②该烧碱溶液的浓度为0.01mol/L
③![]() 的电离平衡常数:b点>a点
的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,取pH=2的两种二元酸H2A与H2B各1 mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述不正确的是
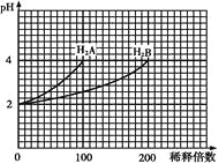
A.H2A为二元强酸
B.pH=4的NaHA水溶液中离子浓度大小为:c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-)
C.含NaHA、NaHB的混合溶液中,离子浓度大小为:c(Na+)=c(A2-)+c(HB-)+c(B2-)+c(H2B)
D.Na2B的水溶液中,离子浓度大小为:c(Na+)>c(B2-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列装置或实验操作正确的是

A. ①用pH试纸测某溶液的酸碱性 B. ②探究氧化性:KMnO4>Cl2>I2
C. ③吸收氨气制氨水 D. ④中和滴定实验
查看答案和解析>>
科目: 来源: 题型:
【题目】向NaOH溶液中缓慢通入![]() 气体,溶液中
气体,溶液中![]() 的物质的量与通入
的物质的量与通入![]() 物质的量的关系图如下。下列关于图中a、b两点溶液的说法错误的是( )
物质的量的关系图如下。下列关于图中a、b两点溶液的说法错误的是( )

A.a、b溶液与同浓度盐酸完全反应时,消耗盐酸的体积相同
B.a溶液中水的电离程度与b溶液中水的电离程度相同
C.a、b两溶液都满足:![]()
D.将a、b两点混合后溶液满足:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】在25℃时,在浓度为1mol/L的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测其c(NH4+)分别为a、b、c(单位为mol/L),下列判断正确的是
A. a=b=c B. a>b>c C. a>c>b D. c>a>b
查看答案和解析>>
科目: 来源: 题型:
【题目】次氯酸可用于杀菌消毒,已知![]() 时:①
时:①![]() 、②
、②![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.在![]() 时,次氯酸的电离方程式及热效应可表示为:
时,次氯酸的电离方程式及热效应可表示为:![]()
B.将![]() 与
与![]() 混合后的溶液,一定存在:
混合后的溶液,一定存在:![]()
C.将![]() 与
与![]() 等体积混合后的溶液,溶液显碱性,则存在:
等体积混合后的溶液,溶液显碱性,则存在:![]()
D.已知酸性![]() ,则等浓度
,则等浓度![]() 和NaClO的混合液中:
和NaClO的混合液中:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子组在室温下可能大量共存的是( )
A.pH=2的溶液:HCO3-、Na+、ClO-、NO3-
B.![]() =106的溶液:Al3+、NH4+、CO32-、S2-
=106的溶液:Al3+、NH4+、CO32-、S2-
C.水电离出的c(H+)=10-4mol/L的溶液:Na+、Fe3+、SO42-、Cl-
D.使石蕊呈红色的溶液:NH4+、NO3-、AlO2-、I-
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:pKa=-lgKa,25℃时,H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1mol·L—1NaOH溶液滴定20mL0.l mol·L—1H2A溶液的滴定曲线如右图所示(曲线上的数字为pH)。下列说法正确的是

A. a点所得溶液中c(H2A)+c(A2—)+c(HA—)=0.1 mol·L—1
B. b点所得溶液中:c(H2A)+2c(H+)=c(A2—)+2c(OH—)
C. 对应溶液的电导率:a<b<c<d
D. 对应溶液水的电离程度:a>b>c>d
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com