
科目: 来源: 题型:
【题目】从某含Br—废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。已知:
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
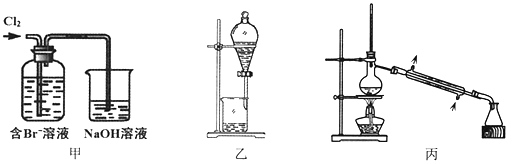
下列说法不正确的是
A. 甲装置中Br—发生的反应为:2Br-+ Cl2 = Br2 + 2Cl-
B. 甲装置中NaOH溶液每吸收0.1mol Cl2,转移0.1mol e—
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2
查看答案和解析>>
科目: 来源: 题型:
【题目】NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×103 ,Ka2=3.9×106)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是

A. 混合溶液的导电能力与离子浓度和种类有关
B. Na+与A2的导电能力之和大于HA的
C. b点的混合溶液pH=7
D. c点的混合溶液中,c(Na+)>c(K+)>c(OH)
查看答案和解析>>
科目: 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.  Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.  正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C.  锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.  使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)青蒿素结构如图,有关叙述正确的是_____(选填序号)。
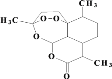
a.化学式为C15H21O5 b.不能与NaOH溶液反应
c.易溶于水 d.含有过氧键,有较强氧化性
由青蒿酸为原料出发,经五步合成可得到青蒿素,其中第2步为还原反应:
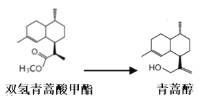
常温下即可反应且略放热,还原剂为LiAlH4。相关物质的性质:
物质 | 性质 |
双氢青蒿酸甲酯(C16H28O2) | 固体,难溶于水,易溶于有机溶剂。 |
青蒿醇(C15H28O) | 固体,难溶于水,易溶于有机溶剂。 |
乙醚 | 无色液体,微溶于水;密度0.71g/cm3;沸点34.6℃。 |
氢化铝锂 | 固体,溶于乙醚。 与水反应:LiAlH4 + 4H2O →Al(OH)3↓+ LiOH +4H2↑ 可将一分子酯还原成二分子醇,自身生成醇铝、醇锂。 (醇铝、醇锂可与盐酸反应,生成铝盐、锂盐和相应的醇)。 |
某学习小组在实验室用双氢青蒿酸甲酯制取青蒿醇。
(2)反应中使用过量的氢化铝锂,理由是_____________________________________________。为使反应在溶液状态下进行,可用乙醚为溶剂,不用水的理由是____________________。
(3)请设计实验室制备装置(画出草图):____________
(4)该反应有机物的转化率约为96%,所得乙醚溶液中含有醇锂、醇铝、双氢青蒿酸甲酯、氢化铝锂。从反应混合物中提取青蒿醇的方法是:
①加_______后分液;
②从乙醚层提取青蒿醇。有多种方法,以下是二种方案:
方案一:蒸发结晶。 方案二:蒸馏析出晶体。
a.这2个方案在析出晶体后都应有残留液,原因是___________________________________。
b.请对这2个方案进行比较_______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如右图。
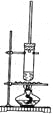
下列对该实验的描述错误的是
A.不能用水浴加热
B.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
C.长玻璃管起冷凝回流作用
D.加入过量乙酸可以提高1-丁醇的转化率
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)碳原子2p亚层上的2个电子不相同的方面是____(选填序号)。
a.能量 b.电子云形状 c.电子云伸展方向 d.自旋状态
14N 原子与12C原子比,质子数和中子数都更多,但原子半径却更小,请解释__________________。
(2)铍(Be)与铝性质相似。
①以下对铍及其化合物的推断肯定不正确的是______(选填序号)。
a.铍会在浓硫酸中钝化 b.氯化铍固体会发生升华现象
c.氧化铍坚硬难熔 d.铍的熔点低于镁
②写出BeCl2溶液和Na2BeO2溶液混合后反应的离子方程式____________________________。
(3)将BeCl2溶液加热蒸干后灼热,再使其熔融,用直流电电解,可得到单质铍和一种单质气体,则该气体的化学式为_______。
(4)氮化铝(AlN)广泛应用于集成电路,其制备原理是将氧化铝与碳粉混合均匀,在持续流动的氮气流中加热至1750℃,发生如下反应:
2Al2O3(s)![]() 4Al(g)+3O2(g) ①
4Al(g)+3O2(g) ①
2C(s)+ O2(g)![]() 2CO(g) ②
2CO(g) ②
2Al(g)+N2(g)![]() 2AlN(s) ③
2AlN(s) ③
试分析反应②对制备AlN的作用______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某次实验室制取乙酸丁酯所用原料为:7.4 mL1-丁醇、6.0 mL冰醋酸,1.0mL浓硫酸。
1-丁醇 | 冰醋酸 | |
密度(g/cm3) | 0.81 | 1.05 |
摩尔质量(g/mol) | 74 | 60 |
若制得乙酸丁酯(式量116)的质量为5.12 g,则以下正确的是
A.产率:约54.49%B.产率:约42.04%
C.转化率:冰醋酸小于1-丁醇D.转化率:冰醋酸大于1-丁醇
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) ![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )

A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
C. 25 ℃时,该反应的平衡常数K=2.2
D. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
查看答案和解析>>
科目: 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是
A. 明矾溶液加热 B. CH3COONa溶液加热
C. 氨水中加入少量NH4Cl固体 D. 小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:链烃A(C5H8)有支链且只有一个官能团。有机化合物A~H的转换关系如下所示:
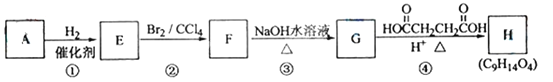
请回答下列问题:
(1)A的结构简式是_________________,名称是________________。
(2)链烃B是A的不同类别的同分异构体,B经催化氢化转化为正戊烷,写出B所有可能的结构简式_________________________________________________________。
(3)写出反应类型:反应②___________________,反应③____________________。
(4)写出反应④的化学方程式:_____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com