
科目: 来源: 题型:
【题目】用惰性电极电解下列溶液一段时间后再加入一定量的某种物质(方括号内物质),能够使溶液恢复到原来的成分和浓度的是( )
A. AgNO3 [AgNO3] B. NaOH [H2O]
C. KCl [KCl] D. CuSO4 [Cu(OH)2]
查看答案和解析>>
科目: 来源: 题型:
【题目】用短线“—”表示共用电子对,用“··”表示未成键孤电子对的式子叫路易斯结构式。R分子的路易斯结构式可以表示为![]() 则以下叙述错误的是( )
则以下叙述错误的是( )
A. R为三角锥形 B. R可以是BF3
C. R是极性分子 D. 键角小于109°28′
查看答案和解析>>
科目: 来源: 题型:
【题目】氢氧化镁:①是中强碱;②广泛用作阻燃剂和填充剂.以白云石(化学式:MgCO3CaCO3)为原料制备氢氧化镁的工艺流程如下:
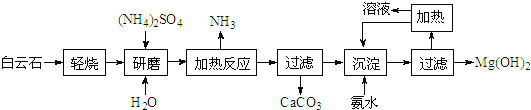
(1)根据流程图,白云石“轻烧”后固体产物的主要成份是MgO和_______(写化学式)。
(2)流程图中“加热反应”有氨气生成的化学方程式为_________________________。
(3)洗涤Mg(OH)2沉淀所用玻璃仪器有:_______、烧杯、玻棒;检验洗净的方法是____________。
(4)传统工艺是将白云石高温分解为氧化镁和氧化钙后提取,而该工艺采用轻烧白云石的方法,其优点是__________________。
(5)25℃时Mg(OH)2饱和溶液的中:c(Mg2+)=2.80×10﹣4mol/L,Mg(O2)22﹣、Mg(OH)42﹣的浓度共为2.35×10﹣4mol/L,则溶液的pH=_______(取整数值);若经过循环利用,每制得5.8t Mg(OH)2时排出200m3的废水,其中Mg2+、Mg(O2)22﹣、Mg(OH)42﹣的浓度共为1.50×10﹣4mol/L,则该工艺的产率为___________(保留4位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】1,6—己二酸是合成高分子化合物尼龙的重要原料之一,可用六个碳原子的化合物氧化制备。下图是合成尼龙的反应流程:
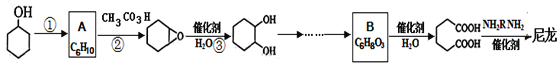
已知:
![]() 2CH3COOH
2CH3COOH
完成下列填空:
(1)写出反应类型:反应①_____反应②__________。
(2)A和B的结构简式为_______、_________。
(3)在上述反应流程的物质中,含氢原子位置不同最多的物质是___________(填名称),最少的物质是________(填结构简式)。
(4)由![]() 合成尼龙的化学方程式为___________。
合成尼龙的化学方程式为___________。
(5)由A通过两步制备1,3—环己二烯的合成线路为:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各关系式中能说明反应N2+3H2![]() 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
A. 3v正(N2)=v正(H2) B. v正(N2)=v逆(NH3)
C. 2v正(H2)=3v逆(NH3) D. v正(N2)=3v逆(H2)
查看答案和解析>>
科目: 来源: 题型:
【题目】Heck反应是偶联反应的一种,例如:反应①如下:
![]() +CH3OOCCH=CH2(Ⅰ)
+CH3OOCCH=CH2(Ⅰ)![]()
![]() (Ⅱ)
(Ⅱ)
化合物I可以由以下途径合成:
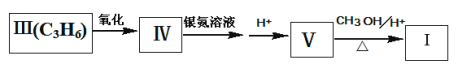
回答以下问题:
(1)化合物Ⅱ的分子式为_____,1mol该物质最多可与________molH2发生加成反应。
(2)卤代烃CH3CHBrCH3发生消去反应可以生成化合物Ⅲ,相应的化学方程式为: ________(注明条件)。
(3)分子式为C4H6O的化合物Ⅵ,满足以下条件:①与化合物IV互为同系物;②含有甲基且无支链,写出其结构简式________。
(4)一定条件下,![]() 与
与 ![]() 也可以发生类似反应①的反应,其有机产物的结构简式为__________。
也可以发生类似反应①的反应,其有机产物的结构简式为__________。
(5)设计一条以CH3CHClCHClCH3和![]() 为原料合成
为原料合成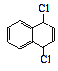 的路线_______。
的路线_______。
提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:(用合成路线流程图表示为:A![]() B……
B……![]() 目标产物)。
目标产物)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现用Pt电极电解1 L浓度均为0.1 mol·L-1的HCl、CuSO4的混合溶液,装置如图,下列说法正确的是( )
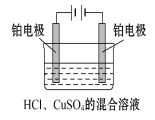
A.电解开始时阴极有H2放出
B.电解开始时阳极上发生:Cu2++2e-Cu
C.整个电解过程中,SO42-不参与电极反应
D.当电路中通过电子的量超过0.1 mol时,此时阴极放电的离子发生了变化
查看答案和解析>>
科目: 来源: 题型:
【题目】流动电池是一种新型电池。其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定。北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4=CuSO4+PbSO4+2H2O。下列说法不正确的是
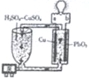
A.a为负极,b为正极
B.该电池工作时PbO2电极附近溶液的pH增大
C.a极的电极反应为Cu-2e-=Cu2+
D.调节电解质溶液的方法是补充CuSO4
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________(填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:

试回答下列问题:
①图1的A中最好选用下列装置_________(填编号);
②图1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;
③图1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;
④某学生按图2进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因_________,其反应的离子方程式是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钠有两种化合物,碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3),其中碳酸钠最为重要,在工业上有广泛的应用。在生活中,碳酸氢钠是常用的发酵剂的主要成分。完成下列计算:
(1)某天然碱的化学组成可能为aNa2CO3bNaHCO3cH2O(a、b、c为正整数),为了确定其成分:称取天然碱样品7.3g,充分加热后得到水的质量为0.9g,二氧化碳的质量为1.1g。该天然碱的化学式为____________。
(2)为了测定某发酵剂样品中碳酸氢钠的含量,取样品n克,充分灼烧以后,称的残留固体质量为m克(假设其他成分不分解)。则样品中碳酸氢钠的质量:_________(填含n、m的计算式)。
(3)已知酸性强弱顺序为:H2CO3 > HCO3- > HX。取由0.4molNaX、0.2molNa2CO3和0.1molNaHCO3组成的混合物,溶于200mL水中,往所得溶液中通入一定量的CO2气体,反应明显分两步,完成下列表格。
CO2(mol) | 0.05 | 0.15 | 0.6 |
NaX(mol) | ____ | ____ | ____ |
Na2CO3(mol) | ____ | ____ | ____ |
NaHCO3(mol) | ____ | ____ | ____ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com