
科目: 来源: 题型:
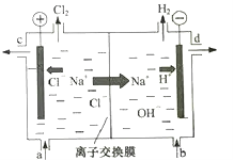
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
完成下列填空:
(1)写出电解饱和食盐水的离子方程式___。
(2)精制饱和食盐水从图中___位置补充,氢氧化钠溶液从图中___位置流出(选填“a”、“b”、“c”或“d”)。
(3)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。
写出该反应的化学方程式___。
(4)室温下,0.1mol/LNaClO溶液的pH___0.1mol/LNa2SO3溶液的pH(选填“大于”、“小于”或“等于”)。
(5)浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为___。
已知:H2SO3:Ki1=1.54×102,Ki2=1.02×107,HClO:Ki1=2.95×108,H2CO3:Ki1=4.3×107,Ki2=5.6×1011。
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积固定的密闭容器中充入一定量的X、Y两种气体,一定条件下发生反应并达到平衡:3X(g)+Y(g)![]() 2Z(g) △H<0。若测得平衡时X的转化率为37.5 %,Y的转化率是X的
2Z(g) △H<0。若测得平衡时X的转化率为37.5 %,Y的转化率是X的![]() ,则下列叙述正确的是
,则下列叙述正确的是
A.升高温度,平衡向正反应方向移动
B.起始时刻n(X) : n(Y)= 2 : 1
C.充入氦气增大容器内的压强,Y的转化率提高
D.若以X表示的反应速率为0.2mol/(L·s),则以Z表示的反应速率为0.3mol/(L·s)
查看答案和解析>>
科目: 来源: 题型:
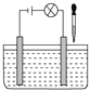
【题目】在如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是( )
A.盐酸中逐滴加入食盐溶液
B.醋酸中逐滴加入氢氧化钠溶液
C.饱和石灰水中不断通入CO2
D.醋酸中逐滴加入氨水
查看答案和解析>>
科目: 来源: 题型:
【题目】金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。完成下列填空:
(1)铝原子核外电子云有___种不同的伸展方向,有___种不同运动状态的电子。
(2)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式___。
(3)硅与铝同周期。SiO2是硅酸盐玻璃(Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成氧化物形式___。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式为___。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为___。
(4)用铝和金属氧化物反应制备金属单质是工业上常用的方法。如:2Al+4BaO![]() 3Ba↑+BaOAl2O3。常温下Al的金属性比Ba的金属性___(选填“强”“弱”)。利用上述方法可制取Ba的主要原因是___。
3Ba↑+BaOAl2O3。常温下Al的金属性比Ba的金属性___(选填“强”“弱”)。利用上述方法可制取Ba的主要原因是___。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaOAl2O3比Al2O3稳定 d.Ba的沸点比Al的低
查看答案和解析>>
科目: 来源: 题型:
【题目】氨水是氨气的水溶液,主要用作化肥。现有25℃时0.1 mol/L的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中的c(NH4+)_________,溶液的pH_________(填“增大”“减小”“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:____________;所得溶液的pH_________7(填“>”、“<”或“=”),用离子方程式表示其原因________。
(3)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺是_______
(4)实验室可用向浓氨水中加入CaO的方法制取氨气,从氨水中存在的平衡入手分析产生NH3的原因:__________
查看答案和解析>>
科目: 来源: 题型:
【题目】生活污水中氮元素是造成水体富营养化的主要原因。若某污水中NH4Cl含量为180 mg/L。
(1)写出NH4Cl的电子式_________。
(2)写出与氯同周期,有2个未成对电子的原子的电子排布式:_______、________
(3)为除去废水中的NH4+,向103 L该污水中加入0.1 mol/L NaOH溶液,理论上需要NaOH 溶液的体积为_________L(计算结果保留两位小数)。
(4)若某污水中同时存在NH4+和NO3-时。可用下列方法除去:可先在酸性污水中加入铁屑将NO3-转化为NH4+后再除去,请配平下列离子方程式并标出电子转移的方向和数目:___Fe +___NO3- +___H+=___Fe2+ +___NH4+ +___H2O,____________。
查看答案和解析>>
科目: 来源: 题型:
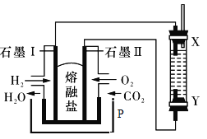
【题目】以H2、O2、熔融盐Na2CO3组成燃料电池,采用电解法制备Fe(OH)2,装置如图所示,其中P端通入CO2,通电一段时间后,右侧玻璃管中产生大量的白色沉淀,且较长时间不变色。则下列说法中正确的是( )
A.X、Y两端都必须用铁作电极
B.不可以用NaOH溶液作为电解液
C.阴极发生的反应是:2H++2e-=H2↑
D.白色沉淀只能在阳极上产生
查看答案和解析>>
科目: 来源: 题型:
【题目】利用反应NO2(g)+SO2(g)![]() SO3(g)+NO(g) △H=-Q kJ/mol(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。完成下列填空:
SO3(g)+NO(g) △H=-Q kJ/mol(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。完成下列填空:
(1)该反应中被氧化是元素是_________;写出该反应的平衡常数表达式:K=_________。增大NO2浓度,平衡常数K_________。(填“增大”、“减小”或“不变”)
(2)若上述反应在密闭容器中进行,能表明反应达到平衡状态的是_________(选填编号)。
a. 混合气体颜色保持不变 b. NO2和NO的体积比保持不变
c. 每消耗1 mol SO2的同时生成1 mol SO3 d. 体系中气体平均摩尔质量保持不变
(3)一定温度下,在容积为V L的容器中发生上述反应,t min内,SO2的物质的量下降了a mol,则这段时间内v(NO2)=_________(用相关字母表示)。
(4)请写出两种能提高平衡转化率的措施____________、______________。
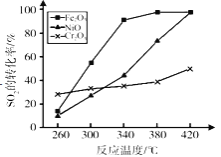
(5)其他条件相同,催化剂不同时,上述反应中SO2的转化率随反应温度的变化如图。不考虑催化剂价格因素,生产中选择Fe2O3作催化剂的主要原因是___________
查看答案和解析>>
科目: 来源: 题型:
【题目】铝是地壳中含量最多的金属元素,铝及其化合物在日常生活、工业上有广泛的应用。
(1)铝原子核外有_________种不同运动状态的电子,有_________种能量不同的电子,写出铝在元素周期表中的位置:________
(2)氮化铝具有强度高,耐磨,抗腐蚀,熔点可达2200℃。推测氮化铝是________晶体,试比较组成该物质的两微粒半径大小:_______
(3)可用铝和氧化钡反应可制备金属钡:4BaO+2Al![]() BaO·Al2O3+3Ba↑的主要原因是_______(选填编号)。
BaO·Al2O3+3Ba↑的主要原因是_______(选填编号)。
a.Al活泼性大于Ba b.Ba沸点比Al的低 c.BaO·Al2O3比Al2O3稳定
(4)工业上用氢氧化铝、氢氟酸和碳酸钠制取冰晶石(Na3AlF6)。其反应物中有两种元素在周期表中位置相邻,可比较它们金属性或非金属性强弱的是_________(选填编号)。
a.气态氢化物的稳定性 b.最高价氧化物对应水化物的酸(碱)性
c.单质与氢气反应的难易 d.单质与同浓度酸发生反应的快慢
(5)描述工业上不用电解氯化铝而是用电解氧化铝的方法获得铝单质的原因:_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com