
科目: 来源: 题型:
【题目】镁及其化合物在工业上有广泛的应用。
完成下列计算:
(1)称取某镁铝合金10g,放入100mL3mol/L的NaOH溶液中,完全反应收集到6.72L的H2(标准状况)。该合金中镁的质量分数为___。
(2)将镁条在空气中燃烧后的产物溶解在50mL1.6mol/L的盐酸中恰好完全反应,再加入过量NaOH把NH3全部蒸发出来,经测定NH3为0.102g,则镁条在空气中燃烧的产物及质量为___。
(3)Mg(HCO3)2溶液加热分解,得到产品轻质碳酸镁。18.2g轻质碳酸镁样品经高温完全分解后得8.0g氧化镁固体,放出3.36L二氧化碳(标准状况),求轻质碳酸镁的化学式___。
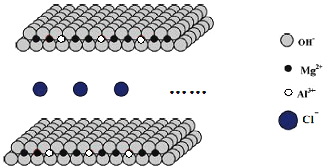
(4)氯离子插层的镁铝水滑石(Mg-Al-ClLDHs)是一种新型的阴离子交换材料。其结构示意图如图所示(每一层可视作平面无限延伸结构)。该离子交换原理是将插层离子与其它阴离子进行等电荷交换。取镁铝水滑石10.66g与0.02molNa2CO3发生完全交换,产物在高温下完全分解,得到金属氧化物和气体。将金属氧化物加入稀硝酸完全溶解后,再加入NaOH溶液直至过量,最终得到4.64g白色沉淀。求Mg-Al-ClLDHs的化学式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组利用下图装置探究温度对氨气还原 Fe2O3 的影响(固定装置略)。完成下列填空:
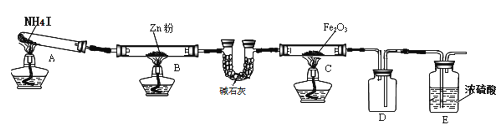
(1)实验时 A 中有大量紫红色的烟气,则 NH4I 的分解产物为 ___(至少填三种),E装置的作用是___。
(2)装置B中的反应方程式:______,D装置的作用是______。
某研究小组按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置 C 加热,反应产物均为黑色粉末(纯净物),两组分别用各自的产物进行以下探究,完成下列填空:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
2 | 取步骤 1 中溶液,滴加 KSCN 溶液 | 变红 | 无现象 |
3 | 向步骤 2 溶液中滴加新制氯水 | 红色先变深后褪去 | 先变红后也褪色 |
(3)乙组得到的黑色粉末是______。
(4)甲组步骤1中反应的离子方程式为______。
(5)乙组步骤3中,溶液变红的原因为______;溶液褪色可能的原因及其验证方法为______。
(6)若装置C中Fe2O3反应后的产物是两种氧化物组成的混合物,为研究氧化物的组成,研究小组取样品7.84克在加热条件下通入氨气,完全反应后,停止加热,反应管中铁粉冷却后,称得质量为5.6克,则混合物的组成为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A.新制的氯水放置一段时间,溶液的pH会减小
B.在配制硫酸亚铁溶液时往往要加入少量铁粉
C.恒容容器中反应CO(g)+NO2(g)![]() CO2(g)+NO(g) △H<0达到平衡后,升高温度,气体颜色变深
CO2(g)+NO(g) △H<0达到平衡后,升高温度,气体颜色变深
D.增大压强,有利于SO2与O2反应生成SO3
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示的各图中,表示2A(g)+B(g)2C(g)(△H<0)这个可逆反应的正确图象为(注:(C)表示C的质量分数,P表示气体压强,C表示浓度)
A. B.
B.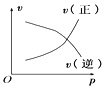 C.
C.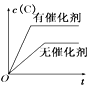 D.
D.
查看答案和解析>>
科目: 来源: 题型:
【题目】将物质的量均为3mol的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)![]() xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,以C表示的平均速率v(C)=0.25molL-1min-1,下列说法正确的是( )
xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,以C表示的平均速率v(C)=0.25molL-1min-1,下列说法正确的是( )
A.反应速率v(B)=0.25molL-1min-1
B.该反应方程式中,x=1
C.2min时,A的物质的量为1.5mol
D.2min时,A的转化率为60%
查看答案和解析>>
科目: 来源: 题型:
【题目】萘普生是重要的消炎镇痛药。以下是它的一种合成路线:
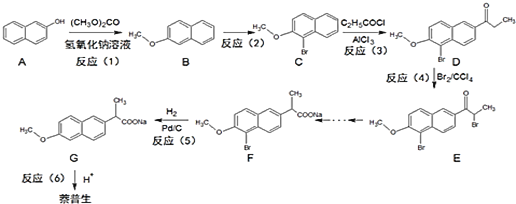
已知:萘(![]() )的化学性质与苯相似。
)的化学性质与苯相似。
完成下列填空:
(1)反应(1)的反应类型是___;A的分子式是___。
(2)反应(2)的试剂和条件是___;反应(3)的产物是D和___(填化学式)。
(3)萘普生不宜与小苏打同时服用的原因是___(用化学方程式表示)。
(4)X是D一种同分异构体,具有以下特点:
①萘的衍生物;②有两个取代基且在同一个苯环上;③在NaOH溶液中完全水解,含萘环的水解产物中有5种化学环境不同的氢。写出X可能的结构简式___。
(5)请用苯和CH3COCl为原料合成苯乙烯。(无机试剂任选)___。
(用合成路线流程图表示为:A![]() B…
B…![]() 目标产物)。
目标产物)。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大 ④保持压强不变,充入N2使容器体积变大
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目: 来源: 题型:
【题目】某地湖盐中含有Ca2+、Mg2+、Fe3+、SO42-等杂质离子,氨碱厂用该地湖盐制取烧碱。其中制得精制食盐水的过程如下:

(1)过程Ⅰ中将粗盐加水溶解需要适当加热,其目的是__________。
(2)过程Ⅱ的目的是除去SO42-,加入的X溶液是__________。
(3)下表是过程Ⅱ、Ⅲ中生成的部分沉淀及其在20℃时的溶解度[g/100gH2O]
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 | Fe(OH)3 |
2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 | 4.8×10-9 |
①过程Ⅲ中生成的主要沉淀除CaCO3和Fe(OH)3外还有__________。
②过程Ⅳ中调节pH时发生的主要反应的离子方程式为__________。
(4)上述精制食盐水中还含有微量的I-、IO3-、NH4+、Ca2+、Mg2+,除去这些离子及进行电解的流程如下:
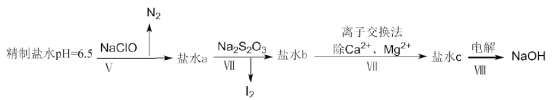
①过程V生成N2的离子方程式为__________。
②过程Ⅳ可以通过控制Na2S2O3的量,将IO3-还原成I2,且盐水b中含有SO42-,该过程中发生氧化还原反应,其中氧化剂和还原剂的物质的量之比为__________。
③在过程Ⅳ中所用的Na2S2O3俗称海波,是一种重要的化工原料。商品海波主要成分是Na2S2O3·5H2O。为了测定其含Na2S2O3·5H2O的纯度,称取8.00g样品,配成250mL溶液,取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol·L-1的碘水滴定(发生反应2S2O32-+I2=S4O62-+2I-),下表记录滴定结果:
滴定次数 | 滴定前读数(mL) | 滴定后读数(mL) |
第一次 | 0.30 | 29.12 |
第二次 | 0.36 | 30.56 |
第三次 | 1.10 | 29.88 |
计算样品的纯度为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铁常用于检测硒、污水处理等。制备FeCl2的方法有多种。
(1)在一定量的盐酸中,逐渐加入一定量的铁屑,若二者恰好完全反应。再向溶液中加入_____________然后保存溶液。
(2)用H2还原无水FeCl3制取FeCl2,装置如下:
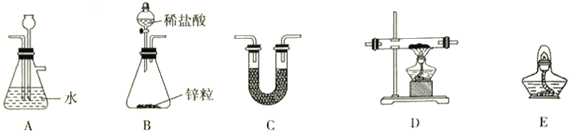
已知:FeCl2、FeCl3易吸水。
①H2还原无水FeCl3制取FeCl2的化学方程式为__________________________________。
②上述仪器的连接顺序为(可多次使用)______________,C中盛放的试剂是___________________。
(3)按下图装置,用162.5g无水氯化铁和225g氯苯,控制反应温度在一定范围加热3h。冷却,分离提纯得到粗产品。反应为2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl。
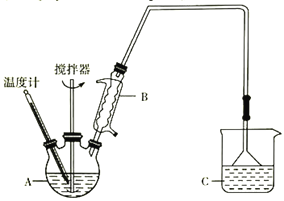
已知:
C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯 | ||
熔点/℃ | -45 | 53 | _________ | _________ |
沸点/℃ | 132 | 173 | _________ | _________ |
①仪器A的名称是____________;下列装置可以代替装置C的是_____________(填字母)。

②反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl中,氧化产物是_________________________。
③反应的温度最好控制在_______________左右。
④反应结束后,冷却实验装置,将仪器A 内物质经过过滤洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是_________________________。
⑤通过烧杯中的现象变化就可以监控氯化铁的转化率。若要监控氯化铁转化率达到或超过80%,则烧杯中试剂为加有酚酞且理论上至少含_______gNaOH的溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:

完成下列填空:
(1)乙中含氧官能团的名称为___。
(2)由甲转化为乙需经下列过程:
![]()
其中反应Ⅰ的反应类型为___,反应Ⅱ的化学方程式为___。设计反应Ⅰ、Ⅱ的目的是___。
(3)欲检验乙中的碳碳双键,可选用的试剂是___。
a.溴水 b.酸性高锰酸钾溶液 c.溴的CCl4溶液 d.银氨溶液
(4)乙经过氢化、氧化得到丙(![]() ),丙有多种同分异构体,符合苯环上有一个取代基的酯类同分异构体有___种,写出其中能发生银镜反应的同分异构体的结构简式___。
),丙有多种同分异构体,符合苯环上有一个取代基的酯类同分异构体有___种,写出其中能发生银镜反应的同分异构体的结构简式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com