
科目: 来源: 题型:
【题目】非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
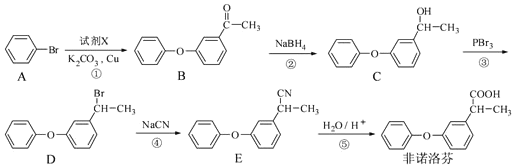
请回答下列问题:
(1)写出非诺洛芬中的含氧官能团的名称___。
(2)反应①中加入的试剂X的分子式为C8H8O2,X的结构简式为___。
(3)在上述五步反应中,属于取代反应的是___(填序号)。
(4)有机物C的一种同分异构体满足下列条件:
Ⅰ.显弱酸性。
Ⅱ.分子中有4种不同化学环境的氢,且分子中含有两个苯环。
写出该同分异构体的结构简式:___。
(5)根据已有知识并结合相关信息,写出以![]() 为原料制备
为原料制备![]() 的合成路线流程图(无机试剂任用)___。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)___。合成路线流程图示例如下:
CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料,已知Pb的化合价只有0、+2、+4。回答下列问题:
(1)PbO2和PbO的混合物中,Pb和O的物质的量之比为8:11,则混合物中,PbO2和PbO的物质的量之比为___。
(2)用足量的CO还原13.7g某铅氧化物,把生成的CO2全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为8.0g,则此铅氧化物的化学式可表示为___。
(3)PbO2具有强氧化性,能氧化浓HCl生成Cl2,+4价的Pb被还原成+2价的Pb,+2价的Pb不具备该性质,据下列信息回答问题:①将amolPbO2加热分解一段时间,生成PbO和O2;②将①所得固体加入足量的浓盐酸,收集产生的Cl2;已知在①加热一段时间后剩余的固体中,+2价的Pb占铅元素质量分数为x;则反应过程中生成的氧气和氯气物质的量总和是多少___?
(4)PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a点为样品失重4.0%((即样品起始质量—a点固体质量)/样品起始质量×100%)的残留固体。若a点固体组成表示为PbOx或mPbO2·nPbO,列式计算x值和m:n值___、___。
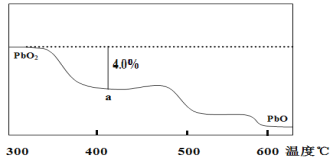
查看答案和解析>>
科目: 来源: 题型:
【题目】将含有苯胺(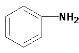 ),水杨酸(
),水杨酸(![]() )、硝基苯与苯酚四种有机物的乙醚溶液,按如图流程利用物质的酸碱性依次分离,假设每一步分离都是完全的。(已知苯胺是一种难溶于水,具有弱碱性的有机物。)
)、硝基苯与苯酚四种有机物的乙醚溶液,按如图流程利用物质的酸碱性依次分离,假设每一步分离都是完全的。(已知苯胺是一种难溶于水,具有弱碱性的有机物。)
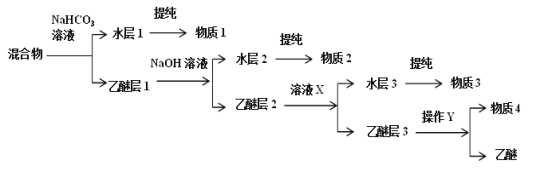
完成下列填空:
(1)水层1中溶解的有机物的结构简为___,物质3的分子式为___。
(2)高中化学实验室制取硝基苯的原料和反应条件分别是___。
(3)操作Y的名称是___,原理是利用___。
(4)医药上可用水杨酸为原料制取乙酰水杨酸(也叫阿司匹林),结构为: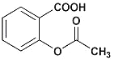 ,请写出两种能鉴别乙酰水杨酸和水杨酸的化学试剂___、___。
,请写出两种能鉴别乙酰水杨酸和水杨酸的化学试剂___、___。
(5)水杨酸可以在一定条件下自身合成高分子化合物,该反应方程式为:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸是一种重要的工业原料,广泛应用于炼油、冶金、染料等工业中。硫酸性质是中学化学学习的重点。
请回答下列问题:
(1)写出中学化学中利用物质与浓硫酸共热产生不同类别的两种气体的名称:___、___。
(2)浓硫酸脱水性实验教材中如下操作:取20g蔗糖置200mL烧杯中,加2mL水,搅拌均匀。再加入20mL98%的浓硫酸,迅速搅拌,静置。实验中,生产大量含SO2、CO2等混合气体。写出产生该混合气体的化学方程式:___。
(3)有学生改进了浓硫酸的脱水性实验(装置如图):
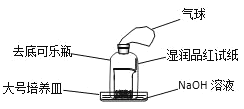
实验准备就绪后,加入浓硫酸,迅速搅拌后用去底可乐瓶罩上,观察现象。除看到烧杯中白色蔗糖颜色变深,体积膨胀,有气体产生外,还可看到哪些现象?___。
(4)图中,仪器a、b的名称分别是___、___;其中,仪器b常用于操作___(填一种物质提纯操作)。

(5)有学生为了确定浓硫酸使蔗糖脱水过程中产生SO2、CO2气体,请选用上述装置(可重复使用)设计实验,将它们的编号填入方框,并将装置内所放的化学药品填入括号内___。
![]()
(浓硫酸,蔗糖)________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个体积为2L的真空密闭容器中加入0.5molCaCO3,发生反应CaCO3(s)![]() CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
CaO(s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线。请按要求回答下列问题:
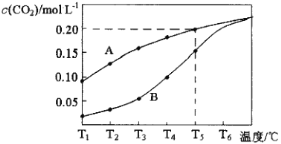
(1)该反应正反应为___(填“吸”或“放”)热反应,温度为T5℃时,该反应耗时40s达到平衡,则T5℃时,该反应的平衡常数数值为___。
(2)如果该反应的平衡常数K值变大,该反应___ (选填编号)。
a.一定向逆反应方向移动 b.在平衡移动时正反应速率先增大后减小
c.一定向正反应方向移动 d.在平衡移动时逆反应速率先减小后增大
(3)请说明随温度的升高,曲线B向曲线A逼近的原因:___。
(4)在T5℃下,维持温度和容器体积不变,向上述平衡体系中再充入0.5molN2,则最后平衡时容器中的CaCO3的质量为___ g。
(5)已知苯酚和碳酸的电离平衡常数如图所示。请写出二氧化碳通入苯酚钠溶液的化学反应离子方程式___,请用电离平衡原理解释上述反应发生的原因以及确定生成物的依据___。
物质 | 电离平衡常数(25℃) |
C6H5OH | Ki=1.28×10-10 |
H2CO3 | Ki1=4.3×10-7 |
Ki2=5.6×10-11 |
查看答案和解析>>
科目: 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O,将12 g该有机物完全燃烧产物通过浓硫酸,浓硫酸增重14.4 g,再通过碱石灰,又增重26.4 g。则该有机物的分子式为( )
A. C4H10 B. C2H6O
C. C3H8O D. C2H4O2
查看答案和解析>>
科目: 来源: 题型:
【题目】某含C、H、O三种元素的有机物M的相对分子质量小于100,经燃烧分析实验测定该有机物碳的质量分数为40%,氢的质量分数为6.7%。由此所得结论正确的是( )
A.M的分子式为CH2O
B.M的实验式为CHO
C.M不可能是2-羟基丙酸
D.M可能是饱和一元羧酸
查看答案和解析>>
科目: 来源: 题型:
【题目】某简单离子的结构示意图可表示为: 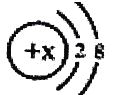 ,当x=8时,该粒子符号为________;当x=11时,该粒子符号为________;当x=13时,写出该粒子的硝酸盐的化学式为________.
,当x=8时,该粒子符号为________;当x=11时,该粒子符号为________;当x=13时,写出该粒子的硝酸盐的化学式为________.
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)与氯元素同族的短周期元素的原子核外电子排布式为___。
(2)能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是___ (填序号)。
a.Cl2、Br2、I2的熔点 b.Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的热稳定性 d.HCl、HBr、HI的酸性
(3)工业上,通过如图转化可制得KClO3晶体:
NaCl溶液![]() NaClO3溶液
NaClO3溶液![]() KClO3晶体
KClO3晶体
II中转化的基本反应类型是___,该反应过程能析出KClO3晶体而无其它晶体析出的原因是___。
(4)晶体硅(熔点1410℃)是良好的半导体材料;四氯化硅熔点-70℃,沸点57.6℃;由粗硅制纯硅过程如图:
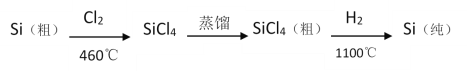
写出SiCl4的电子式:___;在上述由SiCl4制纯硅的反应中,测得生成7kg纯硅需吸收akJ热量,写出该反应的热化学方程式:___。
(5)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目___。
查看答案和解析>>
科目: 来源: 题型:
【题目】前四周期元素A、B、C、D、E原子序数依次增大。已知:A、C同主族,A的原子最外层电子数是次外层的3倍,B的氧化物既能溶于强酸,又能溶于强碱,D的原子半径是第3周期中最小的,E是形成骨骼和牙齿的主要元素,且E单质能和水反应。则下列分析错误的是
A. A的离子结构示意图为![]()
B. D的最高价氧化物的水化物的酸性大于C的最高价氧化物的水化物的酸性
C. E和D形成的离子化合物ED2的电子式为![]()
D. B的氧化物为离子化合物,只含离子键,其晶体为离子晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com