
科目: 来源: 题型:
【题目】某学生为测定未知浓度的硫酸溶液,实验如下:用1.00 mL待测硫酸配制100 mL稀硫酸。以0.12 mol·L-1的NaOH溶液滴定上述稀H2SO4 25.00 mL,滴定终止时消耗NaOH溶液15.00 mL。该学生用标准0.12 mol·L-1 NaOH溶液滴定硫酸的实验操作如下:
A.用蒸馏水洗干净碱式滴定管;
B.检查碱式滴定管是否漏液;
C.用移液管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂;
D.将标准液注入碱式滴定管刻度“0”以上2-3cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下,并记录读数;
E.用标准的NaOH溶液润洗碱式滴定管;
F.按上述操作重复两至三次;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
(1)滴定操作的正确顺序是(用序号填写)__________;该滴定操作中选用的指示剂是酚酞,则在G操作中如何确定滴定终点?____________。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果________ (填“偏小”、“偏大”或“不变”)
(3)滴定前碱式滴定管尖嘴部分有气泡,滴定后气泡消失,则结果会导致测得的稀H2SO4溶液浓度测定值__________(选填“偏大”“偏小”或“无影响”,下同);若滴定前仰视碱式滴定管刻度线,滴定终了俯视刻度线,会使滴定结果__________;
(4)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度__________mol·L-1
(5)写出用稀硫酸中和Ba(OH)2溶液时的离子方程式:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25°C 时,向 10 mL 0.10 mol·L-1 的 HA (Ka =1.0×10-4)中逐滴加入 0.10 mol·L-1NaOH 溶液,溶液 pH 随滴入的 V[(NaOH)aq]变化如下图所示。下列说法正确的是
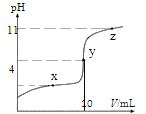
A.x 点,c(HA)> c(A-)
B.y 点,c(HA)+c(A-)=c(Na+) =0.10 mol·L-1
C.z 点,c(Na+) = c(A-) + c(OH-)
D.水的电离程度,x 点小于 y 点
查看答案和解析>>
科目: 来源: 题型:
【题目】描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3H2O | 1.8×10-5 |
下表是常温下几种难(微)溶物的溶度积常数(Ksp):
难(微)溶物 | 溶度积常数(Ksp) |
BaSO4 | 1×10-10 |
BaCO3 | 2.6×10-9 |
CaSO4 | 7×10-5 |
CaCO3 | 5×10-9 |
请回答下列问题:
(l)写出HCN的电离方程式:___________,HClO的电子式__________。
(2)表中所给的四种酸中,酸性最强的是__________(用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大且电离常数改变的操作是__________(填字母序号)。
A.加少量冰酷酸 B.降低温度 C.加水稀释 D.升高温度 E.加少量的CH3COONa固体
(3)CH3COONH4的水溶液呈__________(选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是__________。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BasO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.02 mol·L-1,则溶液中CO32-物质的量浓度应≥__________mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家研制出以石墨烯为载体的催化剂,能在 25℃下,将 CH4 与 H2O2 反应直接转化为含氧有机物,其主要原理如下图所示:
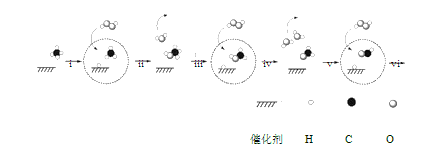
下列说法正确的是
A.步骤 i 中有π键断开
B.上图中![]() 代表甲醇
代表甲醇
C.步骤 ii 中产生的 H2O 分子中的 H 原子都源于 H2O2 分子
D.步骤 i 至 vi 总反应为 CH4+3H2O2![]() CO+5H2O
CO+5H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g)。已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)。已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K=________,该反应是_________反应(填“放热”或“吸热”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe2O3、CO各4.0 mol,反应经过20min后达到平衡。求该时间范围内反应的平均反应速率v(CO)=__________、CO的平衡转化率=__________。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________
A.降低反应温度 B.增加Fe2O3的量 C.加入合适的催化剂 D.移出部分CO2 E.减小容器的容积
(4)在1L的密闭容器中,1150℃条件,下列达平衡状态的是__________。
A | B | C | D | |
n(Fe2O3) | 0.350 | 0.027 | 0.080 | 0.080 |
n(CO) | 0.010 | 0.010 | 0.010 | 0.050 |
n(Fe) | 0.100 | 0.064 | 0.080 | 0.080 |
n(CO2) | 0.035 | 0.088 | 0.037 | 0.050 |
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示为海水综合利用的部分流程,下列有关说法正确的是
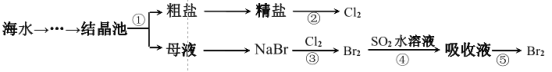
A.实验室进行步骤①需要坩埚、玻璃棒等仪器
B.步骤②是一个将化学能转化为电能的过程
C.步骤③、⑤涉及的化学反应均为氧化还原反应
D.步骤④中的离子方程式为 SO2+Br2+2H2O=4H++SO32-+2Br-
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,把下列各题的结果填在横线上
(1)0.0005 mol/L的氢氧化钡溶液的pH=____________
(2)pH=4的HNO3溶液中,水电离出的H+的物质的量的浓度c(H+)=___________mol·L-1
(3)pH=4的NH4Cl溶液中,水电离出的H+的物质的量的浓度c(H+)=___________mol/L
(4)pH相同的下列溶液:①盐酸、②醋酸,分别与足量且表面积相同的锌片反应,反应起始时生成气体的速率_______(选用“①快”或“②快”或“一样快”或“无法判断”填写),最终生成气体的体积_______。(选用“①多”或“②多”或“一样多”或“无法判断”填写)
(5)用离子方程式表示FeCl3溶液显酸性的原因:___________
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,正确的是
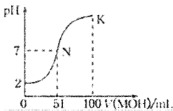
A.HA为一元弱酸
B.MOH为一元强碱
C.N点水的电离程度小于K点水的电离程度
D.K点时,则有c(MOH)+c(OH-)-c(H+)=0.005 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】某酸性溶液中只有Na+、CH3OOO-、H+、OH-四种离子。则下列描述正确的是
A.该溶液可由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
B.该溶液可由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
C.加入NaOH,溶液中离子浓度可能为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
查看答案和解析>>
科目: 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数,下列说法中正确的是
A.1 L 1 mol·L-1 的醋酸溶液中 H+的数目为 NA
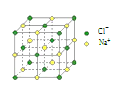
B.4 mol NaCl 晶体中含有右图所示的结构单元的数目为 NA
C.71 g Cl2 通入水中,HClO、Cl-两种粒子数目总和为 2NA
D.标准状况下,22.4 L CHCl3 和 CCl4 的混合物所含有分子数目为 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com