
科目: 来源: 题型:
【题目】肼(N2H4)和氨均为重要的化工原料。回答下列问题:
已知:I.N2H4(l)+O2(g)![]() N2(g)+2H2O(l) △H=-624.0 kJ/mol
N2(g)+2H2O(l) △H=-624.0 kJ/mol
II.N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4 kJ/mol
2NH3(g) △H=-92.4 kJ/mol
III.2NH3(g)![]() N2H4(l)+H2(g) △H=+144.8 kJ/mol
N2H4(l)+H2(g) △H=+144.8 kJ/mol
(1)H2的燃烧热△H=_____________。
(2)T1 °C时,向恒容的密闭容器中加入1 mol N2H4和1 mol O2,发生反应I。达到平衡后,只改变下列条件,能使N2的平衡体积分数增大的是_______( 填选项字母)。
A.增大压强 B.再通入一定量O2
C.分离出部分水 D.降低温度
(3)在恒压绝热的密闭容器中通入一定量的N2和H2,发生反应II和反应III。反应III对N2的平衡转化率的影响为_____(填“增大”“减小”或“无影响”),理由为___________。
(4)t2°C时,向刚性容器中充入NH3,发生反应III。NH3和H2的分压(p)与时间(t)的关系如图所示。
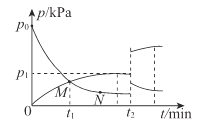
①0~t1min内,反应的平均速率v(NH3)=____kPa/min
②反应的平衡常数Kp=______kPa-1 (Kp为用分压表示的平衡常数)。
③反应物分子的有效碰撞几率:M____N(填“>”“<”或“=”)。
④t2 min时升高温度,再次达到平衡后,H2的分压增大的原因为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】按如图所示装置进行下列不同的操作,
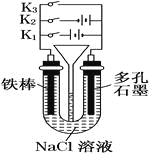
其中不正确的是
A.铁腐蚀的速度由大到小的顺序是:只接通K1>只闭合K3>都断开>只闭合K2
B.只接通K1,一段时间后,U形管中出现白色沉淀
C.只接通K2,U形管左、右两端液面均下降
D.先只接通K1,一段时间后,漏斗液面上升,然后再只接通K2,漏斗液面下降
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:25 °C时,MOH的Kb=10-7。该温度下,在20.00 mL0.1 mol· L-1 MCl溶液中滴入0.1 mol·L-1NaOH溶液,溶液的pH与所加NaOH溶液的体积关系如图所示。下列说法错误的是
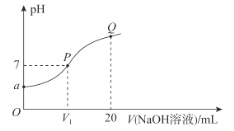
A.a=4B.V1=10
C.溶液中水的电离程度:P>QD.Q点溶液中c(Na+)<2c(M+)
查看答案和解析>>
科目: 来源: 题型:
【题目】用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是
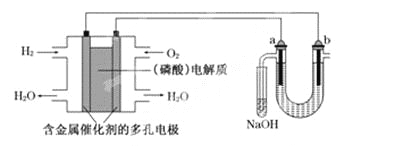
A. 电池工作时,正极反应式为: O2+2H2O+4e-===4OH-
B. 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
C. 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D. 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2
查看答案和解析>>
科目: 来源: 题型:
【题目】微生物燃料电池在净化废水的同时能获得能源或得到有价值的化学产品,图2为其工作原理,图1为废水中Cr2O72-离子浓度与去除率的关系。下列说法不正确的是

A. M为电源负极,有机物被氧化
B. 电池工作时,N极附近溶液pH增大
C. 处理1 mol Cr2O72-时有6 mol H+从交换膜左侧向右侧迁移
D. Cr2O72-离子浓度较大时,可能会造成还原菌失活
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组从富含NaBr的工业废水中提取Br2的过程主要包括:氧化、萃取、分液、蒸馏等步骤。已知:可能用到的数据信息和装置如下。
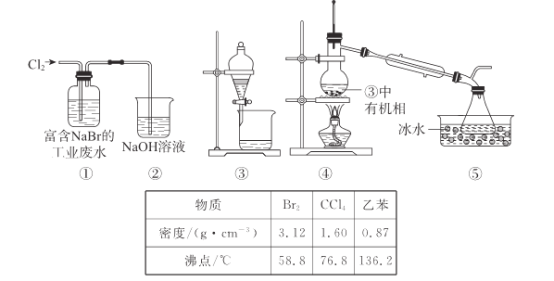
下列说法错误的是
A.实验时,①的废水中出现红色
B.②的作用是吸收尾气,防止空气污染
C.用③进行萃取时,选择CCl4比乙苯更合理
D.④中温度计水银球低于支管过多,导致Br2的产率低
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将pH均为3,体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随1g![]() 的变化如右图所示。下列说法正确的是
的变化如右图所示。下列说法正确的是
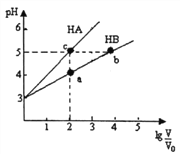
A. 稀释相同倍数时:c(Aˉ)>c(Bˉ-)
B. 水的电离程度:b=c>a
C. 溶液中离子总物质的量:b>c>a
D. 溶液中离子总浓度:a>b>c
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。该电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是( )
A.放电时正极反应为:FeO42-+3e-+4H2O=Fe(OH)3↓+5OH-
B.充电时阴极反应为:Zn(OH)2+2e-=Zn+2OH-
C.放电时每转移3 mol电子,正极有1mol K2FeO4被氧化
D.标有“+”的接线柱充电时作阳极,放电时作正极
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,Ksp(CaSO4)=9×10-4,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。下列判断中正确的是( )
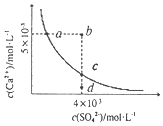
A.a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液
B.向d点溶液中加入适量CaCl2固体可以变到c点
C.a点对应的Ksp不等于c点对应的Ksp
D.b点将有沉淀生成,平衡后溶液中c(SO42-)=3×10-3mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向0.1mol/L的CH3COOH溶液中加少量水,溶液中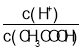 减小
减小
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向盐酸中加入氨水至中性,溶液中![]() >1
>1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() >1
>1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com