
科目: 来源: 题型:
【题目】纳米Fe3O4在生物医学和催化剂载体等领域应用前景光明。其制备流程如下:
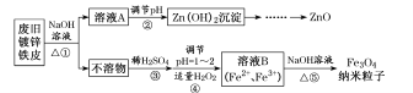
已知:锌单质溶于强碱生成ZnO22-;Zn(OH)2既能溶于强酸又能溶于强碱。
请回答下列问题:
(l)用NaOH溶液处理废旧锌铁皮的作用有___。
A.去除油污 B.溶解镀锌层 C.去除铁锈 D.钝化
(2)步骤②生成Zn(OH)2沉淀的离子方程式为____,用离子方程式结合文字说明该步骤pH不能过小的原因____。调节pH的最佳方法是向溶液中通入____(填化学式)。
(3)步骤④反应的离子方程式为_____;为确保纳米Fe3O4粒子的纯度,应调整原溶液中Fe2+与所加H2O2的物质的量之比为_______。
(4)步骤⑤制得Fe3O4纳米粒子的过程,需要在无氧环境下进行,说明理由__________;T业生产中可采取___________措施提供无氧环境。
(5)步骤⑤ _______(填“能”或“不能”)用减压过滤(抽滤)得到纳米Fe3O4粒子?理由是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如下图所示。反应原理为:CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法正确的是( )
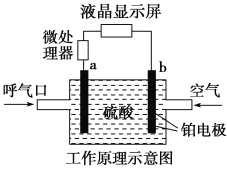
A.电解质溶液中的H+移向a电极
B.b为正极,电极反应式为:O2+4H++4e-=2H2O
C.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
D.呼出气体中酒精含量越高,微处理器中通过的电流越小
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸钾在饮用水源和废水处理过程中,不仅能去除污染物和致癌化学污染物,而且不产生任何诱变致癌的产物,具有高度的安全性;其可溶于水,微溶于浓 KOH 溶液,且在强碱性溶液中比 较稳定。实验室用次氯酸盐氧化法制备高铁酸钾(K2FeO4)的流程如图所示:
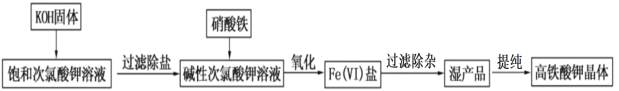
流程图中的饱和次氯酸钾溶液的制备装置如图所示:
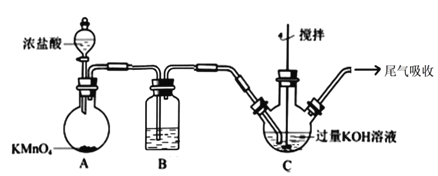
(1)A 为氯气发生装置。A 中反应的离子方程式是___________;装置 B 内的试剂及作用是____________;
(2)装置 C 反应温度控制在 0~5℃进行,在不改变 KOH 溶液浓度前提下,实验中可采取措施是________。
(3)流程图中在加入 KOH 固体的时候会产生大量的白色沉淀_____(填化学式)。
(4)在搅拌下,将 Fe(NO3)3饱和溶液缓慢滴加到 KClO 饱和溶液中即可制取 K2FeO4,写出该反应的离子方程式__________;反应过程中温度控制在 10~15℃,温度过低或过高对反应的影响是_____________。
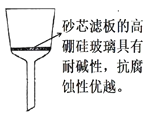
(5)过滤除杂时不用普通漏斗和滤纸而采用砂芯漏斗(如图)的原因是_____________。
(6)在提纯高铁酸钾时采用重结晶、洗涤、干燥的方法,洗涤剂可以选用_____。
A.H2O B.浓 KOH 溶液 C.Fe(NO3)3溶液 D.异丙醇
(7)若提纯得到 a gK2FeO4(M=198g/mol),上述流程中有 5%的 Fe 损失,则需要提供 Fe(NO3)3(M=242g/mol)的质量为_____g(用含 a 的计算式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】示意图甲为锌铜原电池装置,乙为电解熔融氯化钠制备金属钠的装置。 下列说法正确的是
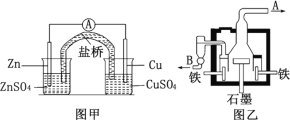
A.甲装置中锌为负极,发生还原反应;铜为正极,发生氧化反应
B.甲装置盐桥可以使反应过程中溶液保持电中性
C.乙装置中铁极的电极反应式为:2Na-2e- = 2Na+
D.乙装置中 B 是氯气出口,A 是钠出口
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是三种难溶金属硫化物的溶度积常数(25℃):
化学式 | FeS | CuS | MnS |
溶度积 | 6.3×10-18 mol2·L-2 | 1.3×10-36 mol2·L-2 | 2.5×10-13 mol2·L-2 |
下列有关说法中正确的是
A.25℃时,CuS 的溶解度大于 MnS 的溶解度
B.除去某溶液中的 Cu2+,可以选用 FeS 作沉淀剂
C.因为 H2SO4 是强酸,所以反应 CuSO4+H2S = CuS↓+H2SO4不能发生
D.25℃时,饱和 CuS 溶液中,Cu2+的浓度为 1.3×10-36 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目: 来源: 题型:
【题目】含氮化合物的用途广泛。 下图表示两个常见固氮反应的平衡常数的对数值(lgK)与温度的关系:①N2+3H22NH3;②N2+O22NO。根据图中的数据判断下列说法正确的是
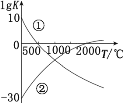
A.反应①和②均为放热反应
B.升高温度,反应①的反应速率减小
C.常温下,利用反应①固氮和利用反应②固氮反应程度相差很大
D.曲线的交点表示反应①和反应②体系中 N2 的浓度一定相等
查看答案和解析>>
科目: 来源: 题型:
【题目】中学化学涉及多种常数。 下列说法正确的是
A.两种物质反应,不管怎样书写化学方程式,平衡常数不变
B.对于反应:3A(g)+2B(g) 4C(s)+2D(g)的化学平衡常数表达式为 K= ![]()
C.KW 不是水的电离平衡常数
D.难溶电解质 AB2 饱和溶液中,c(A2+)=x mol·L-1,c(B-)=y mol·L-1,则 Ksp 值为 4xy2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A.某温度时 N2(g)+3H2(g)![]() 2NH3(g),正、逆反应的平衡常数分别为 K1、K2,则 K1·K2=1
2NH3(g),正、逆反应的平衡常数分别为 K1、K2,则 K1·K2=1
B.若一个可逆反应的化学平衡常数很大,则该反应会在较短的时间内完成
C.氢氧燃料电池是一种将热能转化为电能的装置
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于原子核外电子的描述正确的是
A.s 能级的能量总小于 p 能级的能量
B.2s 的电子云半径比 1s 电子云半径大,说明 2s 的电子比 1s 的多
C.基态铜原子的价电子轨道表示式为 ![]()
D.nf 能级中最多可容纳 14 个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com