
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.碳酸氢钠的水解方程式:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
B.用高锰酸钾标准溶液滴定草酸:2MnO4-+6H++5H2C2O4=2Mn2++10CO2↑+8H2O
C.用碳酸氢钠溶液检验水杨酸中的羧基: +2HCO3-→
+2HCO3-→ +2H2O+2CO2↑
+2H2O+2CO2↑
D.向Na2SiO3溶液中滴加稀盐酸:Na2SiO+2H+=H2SiO3↓+2Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E 为主族元素,A、B、C 同周期且原子半径逐渐减小,A、B 原子的最外层电子数之和等于 C、D 原子的最外层电子数之和。A 元素基态原子的最外层电子排布为 nsnnpn,B 的氢化物可 与其最高价氧化物的水化物反应生成盐。D元素位于元素周期表中长周期,是维持青少年骨骼正常生长发育的重要元素之一,其原子最外层电子数等于最内层电子数。E是元素周期表中原子半径最小的元素。试 回答下列问题:
(1)C 元素基态原子的核外电子排布式是________。
(2)A、B 两元素各有多种氢化物,其电子总数为 10 的氢化物中沸点最高的是________(填化学式)。
(3)B 和 E 可形成离子化合物 BE5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,该物质适当加热就分解成两种气体,试完成:
①该离子化合物的电子式为________。
②该离子化合物溶于水后溶液呈________性(填“酸”“碱”或“中”),其原因是________(用化学方程式表示) 。
(4)下列晶体结构示意图中(黑点表示阳离子,白点表示阴离子),能表示 C 与 D 形成的离子化合物结构的是________(填字母标号 a 或 b)。

查看答案和解析>>
科目: 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示。下列有关P4S3的说法中不正确的是( )
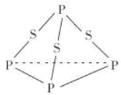
A.P4S3中各原子最外层均满足 8 电子稳定结构
B.P4S3中磷元素为+ 3 价
C.P4S3中 P 原子和 S 原子均为 sp3杂化
D.1molP4S3分子中含有 6mol 极性共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】氯仿![]() 常因保存不慎而被氧化,产生剧毒物光气
常因保存不慎而被氧化,产生剧毒物光气![]() :
:![]() ,下列说法不正确的有
,下列说法不正确的有![]()
![]()

A. ![]() 分子为含极性键的非极性分子
分子为含极性键的非极性分子
B. ![]() 分子中含有3个
分子中含有3个![]() 键、一个
键、一个![]() 键,中心C原子采用
键,中心C原子采用![]() 杂化
杂化
C. ![]() 分子中所有原子的最外层电子都满足8电子稳定结构
分子中所有原子的最外层电子都满足8电子稳定结构
D. 使用前可用硝酸银稀溶液检验氯仿是否变质
查看答案和解析>>
科目: 来源: 题型:
【题目】已知P4单质的结构如下,P4在 KOH 溶液中的变化是:P4 + 3KOH + 3H2O = 3KH2PO2 + PH3 ↑,下列说法正确的是( )
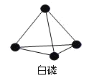
A.产物 PH3分子中所有的原子可能共平面
B.31gP4含有 1.5NA个 P P 键
C.相关元素的电负性大小顺序:P > O > H > K
D.P4中 P 原子为 sp2杂化
查看答案和解析>>
科目: 来源: 题型:
【题目】下列属于氧化还原反应的是( )
A.NH4Cl+NaOH ![]() NH3↑+NaCl+H2O
NH3↑+NaCl+H2O
B.MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C.Na2O2+2H2O=2NaOH+H2O2
D.SO2+H2O=H2SO3
查看答案和解析>>
科目: 来源: 题型:
【题目】轻质碳酸钙是一种广泛应用的工业填料,主要用于塑料、造纸、橡胶和涂料等。工业上以磷石膏(主要成分为CaSO4,杂质主要是SiO2、FeO、Fe2O3、Al2O3等)为原料制备轻质碳酸钙。已知碳酸钙的溶解度比硫酸钙的溶解度小,在一定温度下,钙离子开始沉淀的pH值为12.3,氢氧化铝开始溶解的pH值为12.0,其他金属离子形成氢氧化物沉淀的相关pH的范围如下:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.5 | 2.8 |
Fe2+ | 5.5 | 8.3 |
Al3+ | 3.0 | 4.7 |
制备流程如图:

请问答:
(1)以下说法正确的是__。
A.溶解的过程中,可以用盐酸代替硝酸
B.滤渣1的主要成分是SiO2,滤渣2的上要成分是Fe(OH)3、Al(OH)3
C.转化时,可以先通氨气至饱和后再通过量二氧化碳,以提高钙离子的转化率
D.转化时可以适当加热,以加快反应速率
E.洗涤时可以采用滤液3
(2)调节溶液pH范围时,最佳的pH范围是__,理由是__。
(3)碳酸钙产品中钙含量的测定:
用电子天平准确称量产品2.000g于干净的烧杯中,滴加2mol/L的盐酸恰好完全溶解,加蒸馏水继续蒸发除去过量的酸至pH=6~7,转移至250mL的容量瓶中,定容摇匀。用移液管准确移取25.00mL溶液于锥形瓶中,加入NaOH溶液10mL,摇匀,加入钙指示剂30mg,用已标定的EDTA(乙二胺四乙酸,可以表示为H4Y)标准溶液进行滴定。
已知:Ca2++Y4-=[CaY]2-,测定数据如下:
待测产品溶液体积(mL) | 消耗EDTA标准溶液体积(mL) | EDTA标准溶液的浓度(mol) | |
1 | 25.00 | 14.90 | 0.1121 |
2 | 25.00 | 16.72 | 0.1121 |
3 | 25.00 | 15.00 | 0.1121 |
4 | 25.00 | 15.10 | 0.1121 |
①进行整个滴定操作实验的过程中,下列操作方法正确的是__。
A.使用移液管移取溶液的时候,移液管尖嘴不能接触容器壁
B.滴定管水洗后,需要用标准溶液润洗3次,再排出气泡,使液面位于“0”刻度或“0”刻度以下
C.滴定管调液面后,需静置1~2min,再进行读取刻度数据进行记录
D.电子天平读数时,两边侧面应同时处于打开状态,使空气保持流通
②该产品中钙元素的质量分数为__(保留两位有效数字),若滴定结束时仰视读数,则测定的结果__(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲烷晶体的晶胞结构如图所示,下列说法正确的是( )

A.甲烷晶胞中的球只代表1个C原子
B.晶体中1个CH4分子周围有12个紧邻的CH4分子
C.甲烷晶体熔化时需克服共价键
D.1个CH4晶胞中含有8个CH4分子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对分子性质的解释中,不正确的是( )
A. 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B. 由于乳酸(![]() )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
)中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
C. HF的稳定性很强,是因为其分子间能形成氢键
D. 由右图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子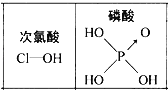
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com