
科目: 来源: 题型:
【题目】利用太阳能光伏电池电解水获得H2,工作示意图如图。下列分析不正确的是( )
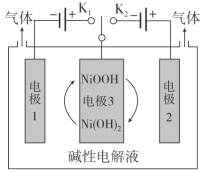
A.控制开关连接K1,电极1发生反应:2H2O+2e-=H2↑+2OH-
B.控制开关连接K2,电极3附近溶液的pH减小
C.通过控制开关连接K1或K2,可交替得到H2和O2
D.电极3的主要作用是通过NiOOH和Ni(OH)2相互转化实现电子转移
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下图所得判断正确的是( )
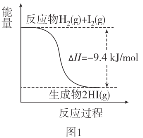
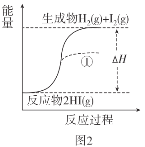
已知:I2(g)=I2(s) ΔH=-62.4kJ/mol
A.图1反应为吸热反应
B.图2反应的热化学方程式为2HI(g)![]() H2(g)+I2(g) ΔH=+9.4kJ/mol
H2(g)+I2(g) ΔH=+9.4kJ/mol
C.图2中若I2的状态为固态,则能量变化曲线可能为①
D.断裂1molH2(g)和1molI2(g)中化学键需要的能量大于断裂2molHI(g)中化学键需要的能量
查看答案和解析>>
科目: 来源: 题型:
【题目】探究铁钉在不同溶液中的腐蚀情况。实验装置与数据如下:
实验装置 | 实验数据 |
|
|
下列说法不正确的是
A.①的负极反应:Fe-3e-=Fe3+
B.③的正极反应:O2+2H2O+4e-=4OH-
C.②可能同时发生析氢腐蚀和吸氧腐蚀
D.金属的电化学腐蚀以哪种类型为主与溶液的pH有关
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案不能达到相应目的的是( )
目的 | A.验证牺牲阳极的阴极保护法 | B.研究浓度对FeCl3水解平衡的影响 |
实验方案 |
|
|
目的 | C.比较CH3COOH和H3BO3(硼酸)酸性的强弱 | D.比较AgCl和AgI溶解度的大小 |
实验方案 |
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列解释事实的方程式不正确的是( )
A.将装有NO2的玻璃球浸入热水中颜色加深:2NO2(g)![]() N2O4(g) ΔH>0
N2O4(g) ΔH>0
B.用Na2S处理含Hg2+废水:Hg2++S2-=HgS↓
C.Na2S2O3溶液与稀H2SO4混合产生浑浊:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O
D.闪锌矿(ZnS)经CuSO4溶液作用转变为铜蓝(CuS):ZnS(s)+Cu2+(aq)=CuS(s)+Zn2+(aq)
查看答案和解析>>
科目: 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是( )
A.100mL1mol/LAl2(SO4)3溶液中,所含Al3+的数目为0.2NA
B.100mL1mol/L氨水中,所含NH![]() 的数目为0.1NA
的数目为0.1NA
C.将1molN2和3molH2充入密闭容器,一定条件下充分反应,得到2NA个NH3分子
D.已知2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ/mol,若反应放出242kJ热量,则形成2NA个共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】锌铜原电池裝置如图所示,下列说法不正确的是( )
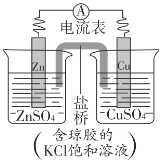
A.锌电极上发生反应:Zn-2e-=Zn2+
B.电子从锌片流向铜片
C.盐桥中K+移向ZnSO4溶液
D.理论上,当6.5gZn溶解时析出6.4gCu
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于反应2SO2(g)+O2(g)2SO3(g)的描述正确的是( )
A.使用催化剂,SO2的平衡转化率增大
B.增大O2浓度,平衡常数K增大
C.当2![]() 正(SO2)=
正(SO2)=![]() 逆(O2)时,反应达到平衡状态
逆(O2)时,反应达到平衡状态
D.升高温度,反应物中活化分子百分数提高,反应速率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】某课题组以苯为主要原料,采取以下路线合成利胆药——柳胺酚。
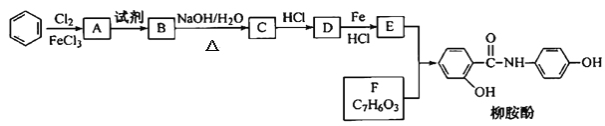
已知:①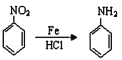
②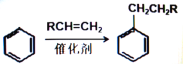 (R为烃基或H原子)
(R为烃基或H原子)
回答下列问题:
(1)对于柳胺酚,下列说法正确的是___(填序号)。
A.1mol柳胺酚最多可以和2molNaOH反应
B.不能发生硝化反应
C.可发生水解反应
D.可与溴发生取代反应
(2)写出A→B反应所需的试剂___。
(3)写出B→C的化学方程式___。
(4)写出化合物F的结构简式____。
(5)写出同时符合下列条件的F的同分异构体的结构简式___(写出1种)。
①属酚类化合物,且苯环上有三种不同化学环境的氢原子;②能发生银镜反应
(6)以苯和乙烯为原料可合成聚苯乙烯,请设计合成路线___(无机试剂及溶剂任选)。
注:合成路线的书写格式参照如下示例流程图:
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】碳化钨(WC)是大型飞机发动机关键部位材料。
(1)基态钨原子的外围电子排布式为5d46s2,有___个未成对电子。
(2)在第二周期的非金属主族元素中,第一电离能由大到小顺序为___。
(3)硫氰化钾(KSCN)俗称玫瑰红酸钾,是铁离子的检验指示剂。
①SCN-中,中心原子碳的杂化类型是___,该离子的空间构型是___。
②SCN-的等电子体分子是___(任写一个)。
(4)C3H8和纯叠氮酸(HN3)的相对分子质量相近,但C3H8常温下是气态,而纯叠氮酸常温下是一种液体,沸点为308.8K,主要原因是___。
(5)NH3的键角是107°,NF3的键角是102.5°。NF3的键角比NH3的键角小,原因是___。
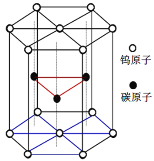
(6)碳化钨晶胞如图所示。①一个W原子与周围___个碳原子紧密相邻且等距。WC的熔点为2870℃,沸点是3000℃,硬度非常大,它的晶体类型是___。
②已知该晶胞边长为acm,高为hcm,NA为阿伏伽德罗常数。WC的摩尔质量为Mg·mol-1。该晶体密度为___g·cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com