
科目: 来源: 题型:
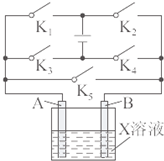 某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:
某课外活动小组准备用如图所示的装置进行实验.现有甲、乙、丙三位同学分别选择了如下电极材料和电解质溶液:| A电极 | B电极 | X溶液 | |
| 甲 | Cu | Zn | H2SO4 |
| 乙 | Pt | Pt | CuCl2 |
| 丙 | Fe | Cu | ? |
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 向20mL硫酸和盐酸的混合溶液中,逐滴加入0.05mol?L-1Ba(OH)2溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图所示.
向20mL硫酸和盐酸的混合溶液中,逐滴加入0.05mol?L-1Ba(OH)2溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图所示.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ||
查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 实验现象 | 结论 |
| ①取部分粉末,加水溶解.将所得溶液分成三份,分别进行实验②③④ | 得无色溶液 | |
| ②滴加稀硫酸 | 无明显现象 | |
| ③滴加氢氧化钠溶液 | 出现白色沉淀 | |
| ④加入足量AgNO3溶液 | 含有NaCl |
查看答案和解析>>
科目: 来源: 题型:阅读理解
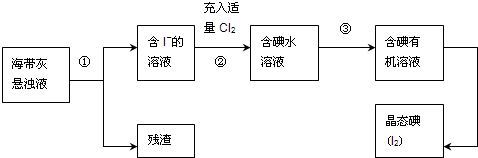
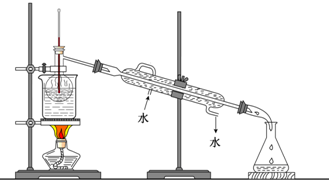
查看答案和解析>>
科目: 来源: 题型:
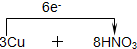 =3Cu(NO3)2+2NO↑+4H2O
=3Cu(NO3)2+2NO↑+4H2O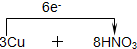 =3Cu(NO3)2+2NO↑+4H2O
=3Cu(NO3)2+2NO↑+4H2O查看答案和解析>>
科目: 来源: 题型:
| 2mNA |
| M |
| 2mNA |
| M |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com