
科目: 来源: 题型:阅读理解
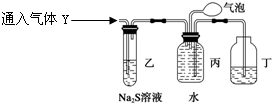 (2011?宣城二模)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动:
(2011?宣城二模)某校化学兴趣小组为了探究粗铁粒(含有少量金属铜杂质)与某浓度硝酸反应,设计了如下探究活动:| 实验步骤 | 现象 | 结论 | 离子方程式 |
| 第一步 | 取2-3mL溶液装于试管,向试管中加入几滴KSCN溶液. | 若溶液变红色,则溶液含有Fe3+; 若无现象,则不含Fe3+ 若溶液变红色,则溶液含有Fe3+; 若无现象,则不含Fe3+ |
Fe3++3SCN-=Fe(SCN)3 Fe3++3SCN-=Fe(SCN)3 |
| 第二步 | 另取少量溶液装于试管,向试管里滴加几滴酸性高锰酸钾溶液 另取少量溶液装于试管,向试管里滴加几滴酸性高锰酸钾溶液 |
若溶液紫色褪去,则溶液含有Fe2+; 若无明显变化,则不含Fe3+. |
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:

 +O2
+O2| 催化剂 |

 +O2
+O2| 催化剂 |

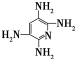 +n
+n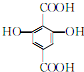
| 催化剂 |
 +(2n─1)H2O
+(2n─1)H2O +n
+n
| 催化剂 |
 +(2n─1)H2O
+(2n─1)H2O查看答案和解析>>
科目: 来源: 题型:
| 元素 | 信息 |
| A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | B原子得一个电子后2p轨道全满 |
| C | C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大 |
| D | D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于其中子数 |
| E | E+和B-具有相同的电子层结构 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
(2011?宣城二模)T℃时,在1L的密闭容器中充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),△H=-49.0kJ?mol-1测得H2和CH3OH(g)的浓度随时间变化如下图所示.下列说法不正确的是( )
|
查看答案和解析>>
科目: 来源: 题型:
 (2011?宣城二模)2011年3月11日,日本本州岛仙台港发生9.0级地震,地震引发海啸,食盐、蔗糖、醋酸、“84消毒液”、明矾等是灾后居民日常生活中经常使用的物质,下列有关说法或表示正确的是( )
(2011?宣城二模)2011年3月11日,日本本州岛仙台港发生9.0级地震,地震引发海啸,食盐、蔗糖、醋酸、“84消毒液”、明矾等是灾后居民日常生活中经常使用的物质,下列有关说法或表示正确的是( )查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com