
科目: 来源: 题型:
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
提纯下列物质(括号内的物质是杂质)所选用的除杂试剂和分离方法都正确的是( )
|
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色K2FeO4和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色Na2FeO4溶液 |
 △
△查看答案和解析>>
科目: 来源: 题型:







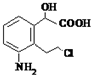 有机物互为同分异构体
有机物互为同分异构体查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com