
科目: 来源: 题型:
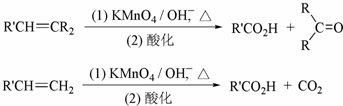
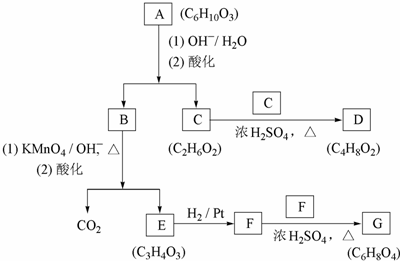
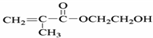



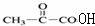
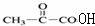


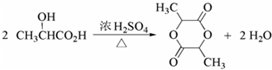

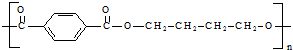 H)是一种最重要的工程塑料之一.
H)是一种最重要的工程塑料之一.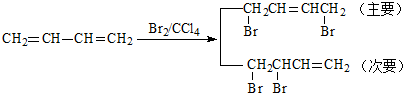
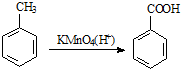
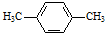 为原料合成PBT;请用反应流程图表示,并注明反应条件.
为原料合成PBT;请用反应流程图表示,并注明反应条件.| 浓H2SO4 |
| 170℃ |
| 高温、高压 |
| 催化剂 |
 CH2-CH2
CH2-CH2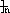


查看答案和解析>>
科目: 来源: 题型:阅读理解
| 沸腾炉温度/℃ | 560 | 580 | 600 | 620 | 640 | 660 |
| 生成物中含水溶性铜化合物的百分含量/% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| 生成物中含酸溶性铜化合物的百分含量/% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 |
查看答案和解析>>
科目: 来源: 题型:
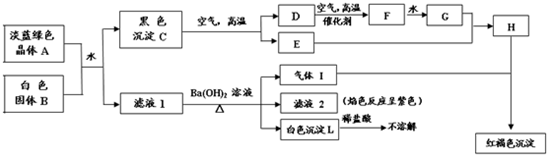
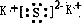
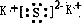
| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
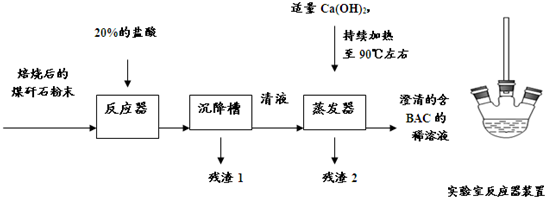
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
已知25℃时有关弱酸的电离平衡常数:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com