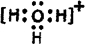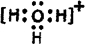用图示装置制取PCl
3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃).已知:PCl
3和PCl
5遇水强烈反应,它们熔沸点数据如下:
|
熔点 |
沸点 |
| PCl3 |
-112℃ |
75℃ |
| PCl5 |
148℃ |
200℃ |
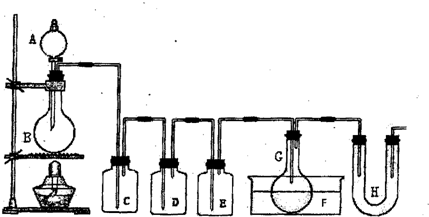
请根据图中装置回答下列问题:
(1)检查该装置气密性的方法是
H接一导管放入水槽,然后微热圆底烧瓶B,若导管口产生气泡,撤灯后导管中形成水柱,说明装置气密性良好.
H接一导管放入水槽,然后微热圆底烧瓶B,若导管口产生气泡,撤灯后导管中形成水柱,说明装置气密性良好.
.
(2)为得到氯气,若B中加入MnO
2,则A中应加入
浓盐酸
浓盐酸
,发生反应的化学方程式为
MnO
2 +4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
MnO
2 +4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
.
(3)若发现C中气泡产生过猛,需要进行的操作的关键是
用分液漏斗控制滴加液体的量或滴加速率
用分液漏斗控制滴加液体的量或滴加速率
.
(4)在反应开始时主要生成PCl
3,而后来主要生成PCl
5,原因可能是
前期P过量生成三氯化磷,后期氯气过量生成五氯化磷
前期P过量生成三氯化磷,后期氯气过量生成五氯化磷
;从PCl
3和PCl
5的混合物中分离也PCl
3的最佳方法是
a
a
(选填序号).
a.蒸馏b.分液c.升华
(5)生成的PCl
3在G中收集,则F中盛有
冷水
冷水
,作用是
使得三氯化磷液化
使得三氯化磷液化
(6)C、D、H所盛的试剂分别是:C
饱和食盐水
饱和食盐水
;D
浓硫酸
浓硫酸
;H
碱石灰
碱石灰
.
(7)如果E中反应放热较多,G处的导管可能发生堵塞,其原因是
五氯化磷蒸汽冷却后变成固体
五氯化磷蒸汽冷却后变成固体
.


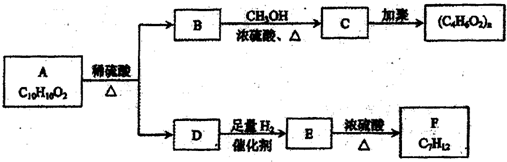


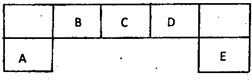 短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,其中B元素形成的化合物在自然界中的种类最多.请回答下列问题
短周期元素A、B、C、D、E在元素周期表中的位置如下图所示,其中B元素形成的化合物在自然界中的种类最多.请回答下列问题