
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、用纯碱溶液吸收合成氨工业尾气 | B、回收炼铁高炉气中的CO来做燃料 | C、用烧碱溶液吸收硝酸工业尾气 | D、用氨水吸收硫酸工业尾气中的SO2 |
查看答案和解析>>
科目: 来源: 题型:
| A、⑥④⑤②③① | B、④⑥⑤②③① | C、⑥④②⑤③① | D、⑥④⑤②①③ |
查看答案和解析>>
科目: 来源: 题型:
| A、燃煤中加人适量石灰石,可减少废气中SO2的量 | B、高纯度的硅单质广泛用于制作光导纤维 | C、为防止电池中的重金属污染土壤和水体,应积极开发废旧电池的综合利用技术 | D、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
查看答案和解析>>
科目: 来源: 题型:
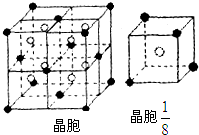
| 1 | 8 |
查看答案和解析>>
科目: 来源: 题型:
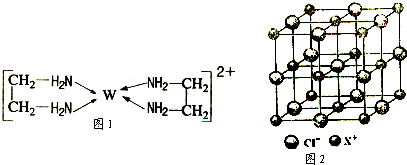
查看答案和解析>>
科目: 来源: 题型:
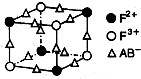 【化学--选修3物质结构与性质】
【化学--选修3物质结构与性质】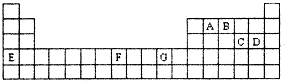
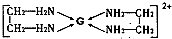 该配离子中含有的化学键类型有
该配离子中含有的化学键类型有| 1 | 8 |
查看答案和解析>>
科目: 来源: 题型:
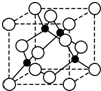
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com