
科目: 来源: 题型:
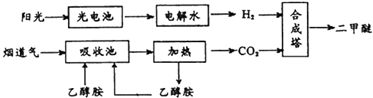
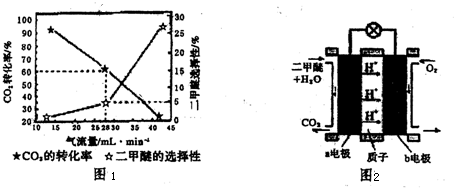
查看答案和解析>>
科目: 来源: 题型:
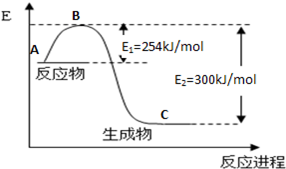 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,| 化学键 | H-H | N≡N |
| 键能/kJ?mol-1 | 435 | 943 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
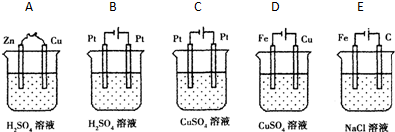
查看答案和解析>>
科目: 来源: 题型:
| A、钢铁腐蚀时可能发生的正极反应:4OH--4e-═2H2O+O2↑ | ||||||
| B、表示中和热的离子方程式:H++OH-═H2O;△H=-57.3kJ/mol | ||||||
| C、明矾水解反应的离子方程式:Al3++3H2O═Al(OH)3+3H+ | ||||||
D、硫酸铵溶液与氢氧化钠溶液混合共热的离子方程式:N
|
查看答案和解析>>
科目: 来源: 题型:阅读理解
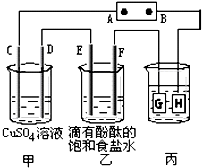 (Ⅰ)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
(Ⅰ)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).查看答案和解析>>
科目: 来源: 题型:
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/( kJ?mol-1) | -283.0 | -285.8 | -726.5 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com