
科目: 来源: 题型:
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/( kJ?mol-1) | -283.0 | -285.8 | -726.5 |
查看答案和解析>>
科目: 来源: 题型:阅读理解
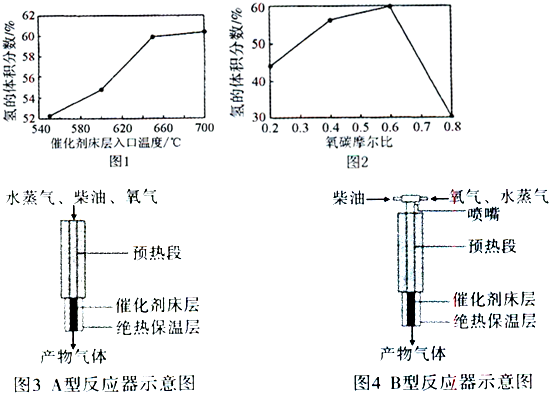
查看答案和解析>>
科目: 来源: 题型:
 (1)美国“阿特兰蒂斯号”航天飞机与2009年5月11日升空修复含勃望远镜,它使用的燃料是液氢和液氧.已知下列热化学方程式:
(1)美国“阿特兰蒂斯号”航天飞机与2009年5月11日升空修复含勃望远镜,它使用的燃料是液氢和液氧.已知下列热化学方程式:| 1 | 2 |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 2 |
| 催化剂 |
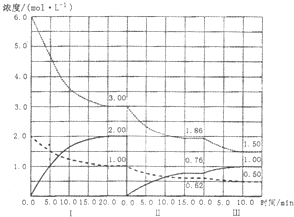
查看答案和解析>>
科目: 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
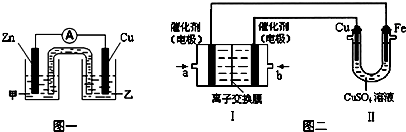
查看答案和解析>>
科目: 来源: 题型:
| 实验编号 | T/K | 催化剂的用量/g | 酸性KMnO4溶液的浓度/mol?L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a.实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; b.实验①和 c.实验①和④探究 |
| ② | 0.5 | 0.001 | ||
| ③ | 323 | 0.010 | ||
| ④ | 298 | 0 | 0.010 |
查看答案和解析>>
科目: 来源: 题型:
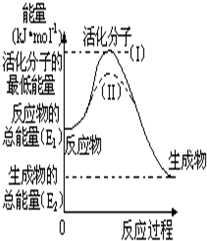 在化学反应中,只有能量比平均能量高的反应物分子发生碰撞时才能发生化学反应.我们把能引发化学反应的碰撞称为有效碰撞,发生有效碰撞的分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位用kJ?mol-1表示.认真观察图,然后回答问题.
在化学反应中,只有能量比平均能量高的反应物分子发生碰撞时才能发生化学反应.我们把能引发化学反应的碰撞称为有效碰撞,发生有效碰撞的分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位用kJ?mol-1表示.认真观察图,然后回答问题.查看答案和解析>>
科目: 来源: 题型:
| 物质 | △H(kJ?mol-1) | 物质 | △H(kJ?mol-1) |
| C(s) | -393.5 | C2H6(g) | -1559.8 |
| H2(g) | -285.8 | C3H8(g) | -2219.9 |
| C2H4(g) | -1411.0 | C12H26(l) | -8162.0 |
查看答案和解析>>
科目: 来源: 题型:
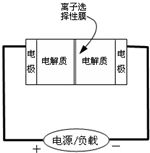 由硫可制得多硫化钠Na2Sx,x的值一般为2~6.当x=2时,多硫化钠称为过硫化钠.
由硫可制得多硫化钠Na2Sx,x的值一般为2~6.当x=2时,多硫化钠称为过硫化钠.| 放电 | 充电 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com