
科目: 来源: 题型:
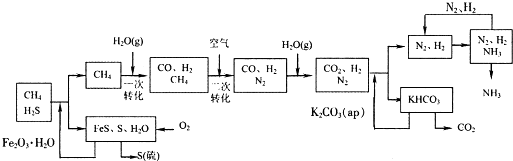
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目: 来源: 题型:
| 催化剂 |
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
查看答案和解析>>
科目: 来源: 题型:
 工业合成氨与制备硝酸一般可连续生产,流程如下:
工业合成氨与制备硝酸一般可连续生产,流程如下: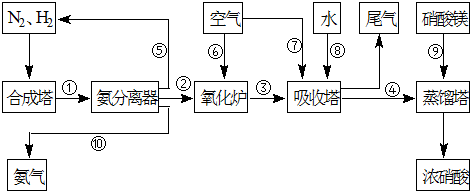
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目: 来源: 题型:
| 1 | 4 |
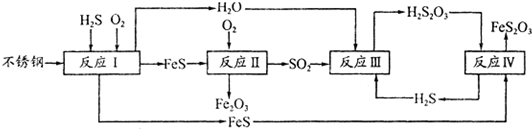
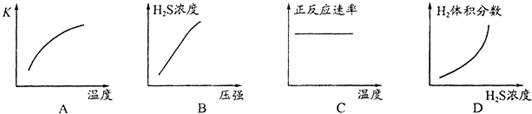
查看答案和解析>>
科目: 来源: 题型:阅读理解
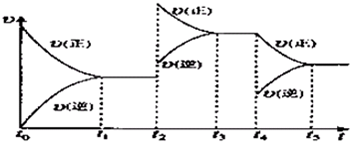
| 15 | 16 |
查看答案和解析>>
科目: 来源: 题型:
| m |
| n |
| m |
| n |
查看答案和解析>>
科目: 来源: 题型:
| A、用过氧化氢制取氧气时,加入催化剂可使氧气的质量增加 | B、催化剂只能加快其他物质的反应速率 | C、化学性质改变 | D、本身的质量和化学性质不会改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com