
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
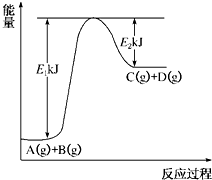 已知某反应A(g)+B(g)?C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:
已知某反应A(g)+B(g)?C(g)+D(g)进行过程中的能量变化如图所示,请回答下列问题:| A | B | C | D | |
| 甲 | a mol | a mol | 0 | 0 |
| 乙 | 2a mol | a mol | 0 | 0 |
| 丙 | a mol | a mol | a mol | a mol |
| 丁 | a mol | 0 | a mol | a mol |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 在100℃时,将0.40mol的二氧化氮气体充入2L真空的密闭容器中,每隔一段时间就对该容器内的物质进行分析,得到数据如表所示:
在100℃时,将0.40mol的二氧化氮气体充入2L真空的密闭容器中,每隔一段时间就对该容器内的物质进行分析,得到数据如表所示:| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
A、X的正反应速率是Y的逆反应速率的
| ||
| B、通入稀有气体He使体系压强增大,平衡将正向移动 | ||
| C、降低温度,混合气体的平均相对分子质量变小 | ||
| D、增加X的物质的量,Y的转化率降低 |
查看答案和解析>>
科目: 来源: 题型:
| 压强 MPa 转化率/% 温度℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
| A、温度一定时增大压强,SO2的转化率增大 |
| B、SO2转化为SO3,最好采用600℃的温度 |
| C、用催化剂不能增大SO2的转化率,但能增加反应放出的热量 |
| D、SO2尾气可用氨水吸收 |
查看答案和解析>>
科目: 来源: 题型:
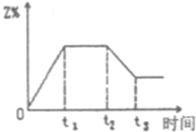 一定条件下,向某密闭容器中加入2molX发生如下反应:2X(g)?2Y(g)+Z(g)△H<0,在t1时刻达到平衡,然后在t2时刻改变某条件,到t3时刻又建立平衡,Z的百分含量变化如图所示,则t2时刻改变的条件是( )
一定条件下,向某密闭容器中加入2molX发生如下反应:2X(g)?2Y(g)+Z(g)△H<0,在t1时刻达到平衡,然后在t2时刻改变某条件,到t3时刻又建立平衡,Z的百分含量变化如图所示,则t2时刻改变的条件是( )| A、升高温度 | B、减小压强 | C、恒压条件下加入2molX | D、加入催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com