
科目: 来源: 题型:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | D | E | |||||
| 3 | B | F | G | |||||
| 4 | A |
查看答案和解析>>
科目: 来源: 题型:
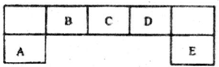
查看答案和解析>>
科目: 来源: 题型:阅读理解
| T/℃t/min pH | 3.0 | 4.0 | 5.0 | 6.0 | 20 | 301 | 231 | 169 | 58 | 30 | 158 | 108 | 48 | 15 | 50 | 31 | 26 | 15 | 7 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
查看答案和解析>>
科目: 来源: 题型:
| 周期 主族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | C | N | O | F | ||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
查看答案和解析>>
科目: 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | N2+3H2?2NH3是放热反应 | 工业合成氨的反应在高温下进行 |
| B | 钠原子核外电子数比铝少 | 钠的金属性比铝强 |
| C | 碳可置换出二氧化硅中的硅 | 碳的非金属性比硅强 |
| D | SO2具有还原性 | SO2能使酸性KMnO4溶液褪色 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目: 来源: 题型:
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
| A、C2+与B3+的核外电子数不可能相等 |
| B、单质与稀盐酸反应的速率A<B |
| C、最高价氧化物对应水化物的碱性A<C |
| D、氢化物的稳定性H2D<H2E |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com