
科目: 来源: 题型:
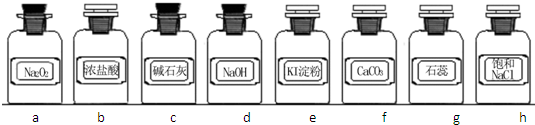
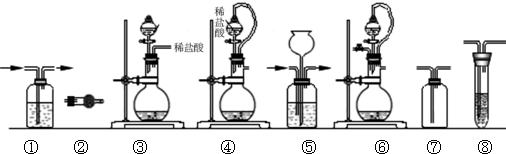
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③、⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ④、⑥ | ⑤ | ⑧/g | ① |
查看答案和解析>>
科目: 来源: 题型:
下列选项中有关物质性质实验得到的结论正确的是( )
|
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目: 来源: 题型:
| A | B | C | D | |
| 实验 | 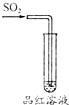 |
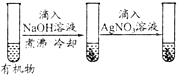 |
 |
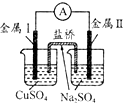 |
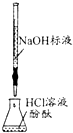
| 现象 | 品红褪色 | 最后试管有浅黄色沉淀 | 最后一滴标液使酚酞由无色变为红色,且30秒不复原 | 盐桥左端从无色逐渐变为蓝色 |
| 结论 | SO2有强氧化性 | 有机物中含有溴原子 | 滴定达到终点 | 金属Ⅱ比Ⅰ活泼 |
查看答案和解析>>
科目: 来源: 题型:
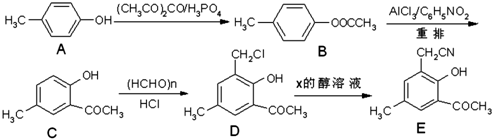
| H+ | H2O |
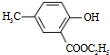 的合成路线流程图,(无机试剂任用).流程图示例如下:
的合成路线流程图,(无机试剂任用).流程图示例如下: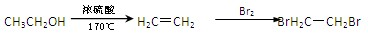
查看答案和解析>>
科目: 来源: 题型:
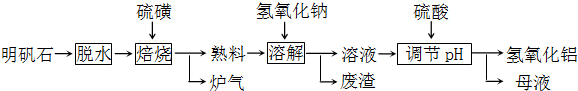
| ||
查看答案和解析>>
科目: 来源: 题型:
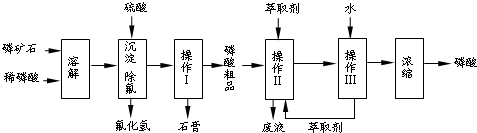
查看答案和解析>>
科目: 来源: 题型:阅读理解
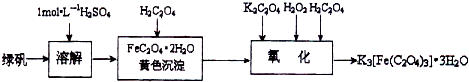
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com