
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
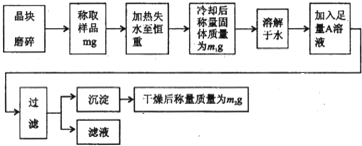
| 阳离子 | 实验操作过程 | 实验现象 |
| K + | 用铂丝蘸取少许待测液,在酒精灯上灼烧,并透过蓝色钴玻璃观察 | |
| Al3+ | 实验操作过程: |
现象: 离子方程式: |
查看答案和解析>>
科目: 来源: 题型:
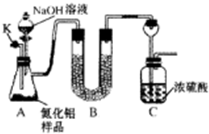 新型陶瓷氮化铝可用Al2O3高温还原法制备:Al2O3+3C+N
新型陶瓷氮化铝可用Al2O3高温还原法制备:Al2O3+3C+N
| ||
查看答案和解析>>
科目: 来源: 题型:
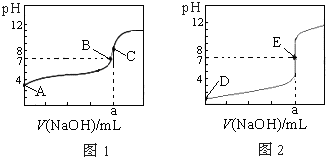 如图为常温下用0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1盐酸和20.00mL 0.1000mol?L-1醋酸的曲线.若以HA表示酸,下列判断和说法正确的是( )
如图为常温下用0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1盐酸和20.00mL 0.1000mol?L-1醋酸的曲线.若以HA表示酸,下列判断和说法正确的是( )| A、图1是滴定盐酸的曲线 | B、B、E状态时,两溶液中离子浓度均为c(Na+)=c(A-) | C、C、E状态时,反应消耗的酸n(CH3COOH)=n(HCl) | D、当0 mL<V(NaOH)<20.00 mL时,对应溶液中各离子浓度大小顺序一定均为c(A-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目: 来源: 题型:
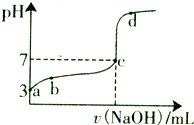 常温下,向20mL 0.1moL/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法不正确的是( )
常温下,向20mL 0.1moL/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法不正确的是( )| A、a点表示的溶液中c(OH-)=10-11mol/L | ||
B、a、b点表示的溶液中
| ||
| C、c点表示CH3COOH和NaOH恰好完全反应c(CH3COOH)?c(OH-) | ||
| D、d点表示的溶液中c(Na+)>c(CH3COO-) |
查看答案和解析>>
科目: 来源: 题型:
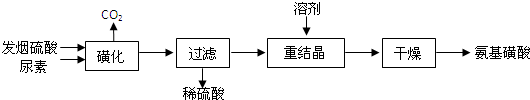
查看答案和解析>>
科目: 来源: 题型:阅读理解
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水成分搅拌、过滤,得滤液A和沉淀B. | / |
| 步骤2: |
|
| 步骤3: |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 实验步骤 | 预期现象和结论 | 步骤1:取适量牙膏样品加水充分搅拌、过滤,得滤液A和沉淀B. | / | 步骤2:取适量滤液A于试管中, |
有 |
步骤3:取适量沉淀B于试管中,加入过量 |
/ | 步骤4:往所得滤液中通入过量二氧化碳. | 产生成白色沉淀, |
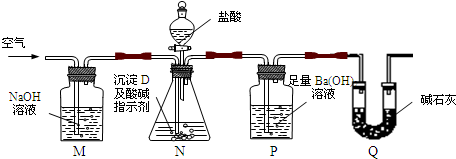
查看答案和解析>>
科目: 来源: 题型:阅读理解

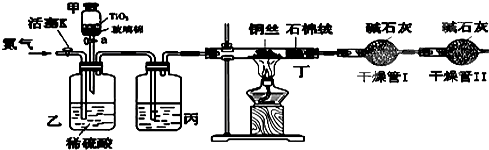
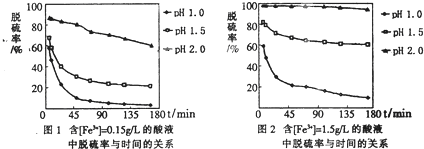
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com