
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| … | A | |||||
| B | C | D |
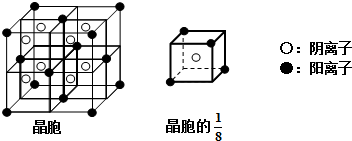
查看答案和解析>>
科目: 来源: 题型:
| A-B | A=B | A≡B | ||||
CO |
键能(KJ/mol) | 357.7 | 798.9 | 1071.9 | ||
| 键能差值(KJ/mol) | 441.2 | 273 | ||||
| N2 | 键能(KJ/mol) | 154.8 | 418.4 | 941.7 | ||
| 键能差值(KJ/mol) | 263.6 | 523.3 | ||||
查看答案和解析>>
科目: 来源: 题型:
| 微粒代码 | 所含原子核个数 | 所带电荷数 |
| A | 1 | 0 |
| B | 4 | 0 |
| C | 多个 | 0 |
| D | 1 | 一个单位正电荷 |
| E | 多个 | 一个单位正电荷 |
| F | 1 | 两个单位正电荷 |
| G | 2 | 一个单位负电荷 |
查看答案和解析>>
科目: 来源: 题型:
| X | Y | |
| 第一电离能(KJ/mol) | 495.8 | 418.8 |
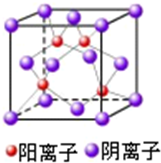
查看答案和解析>>
科目: 来源: 题型:
| J | ||||
| R |
| A、J和氢组成的化合物分子中只含有极性共价键 |
| B、工业上用电解M和T组成的化合物来制备M |
| C、R、T两元素的气态氢化物中,T的气态氢化物更稳定 |
| D、J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4 |
查看答案和解析>>
科目: 来源: 题型:
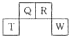 短周期元素Q、P、T、W在元素周期表中的位置如图所示,其中Q的原子序数为其周期序数的3倍.下列叙述错误的是( )
短周期元素Q、P、T、W在元素周期表中的位置如图所示,其中Q的原子序数为其周期序数的3倍.下列叙述错误的是( )| A、QW2是含极性键的非极性分子 | B、四种元素的最高价氧化物能与强碱反应 | C、RHn在同族元素的气态氢化物中沸点最低 | D、R、W常见单质的晶体类型相同 |
查看答案和解析>>
科目: 来源: 题型:
| W | X | ||
| Y | Z |
| A、原子半径:Z<X |
| B、氢化物的稳定性:X<W |
| C、最高价氧化物对应水化物的酸性:Z<Y |
| D、Y的最高化合价和最低化合价的代数和为0 |
查看答案和解析>>
科目: 来源: 题型:
| A、甲、乙、丙、丁四种元素均为短周期元素 | B、气态氢化物的稳定性:甲>乙 | C、最高价氧化物对应的水化物的酸性:甲<丙 | D、元素丁与乙形成的化合物都是非极性分子 |
查看答案和解析>>
科目: 来源: 题型:
下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是( )
|
| A、气态氢化物的稳定性为H2T<H2R |
| B、单质与稀盐酸反应的速率为L<Q |
| C、M与T形成的化合物具有两性 |
| D、L2+与R2-的核外电子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com