
科目: 来源: 题型:
A、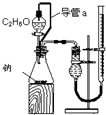 测定乙醇结构 | B、 滴定法测定硫酸的物质的量浓度 | C、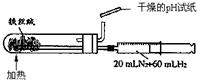 合成氨并检验氨的生成 | D、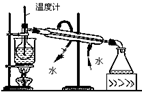 碘的CCl4溶液中分离I2并回收CCl4 |
查看答案和解析>>
科目: 来源: 题型:
| A、浅紫色 | B、黄色 | C、红色 | D、无色 |
查看答案和解析>>
科目: 来源: 题型:
 取m1g某常见粉末(由M、Z两种元素组成)进行如下实验.将该粉末和足量碳粉充分混合,平铺在反应管a中,b瓶中盛足量澄清石灰水.按图连接仪器并检查好气密性.
取m1g某常见粉末(由M、Z两种元素组成)进行如下实验.将该粉末和足量碳粉充分混合,平铺在反应管a中,b瓶中盛足量澄清石灰水.按图连接仪器并检查好气密性.查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 预期现象与结论 | 有关反应离子方程式 |
| 步骤1:从小烧杯中取少量融雪剂溶液,分别置于A、B试管中. | ||
| 步骤2: |
||
| 步骤3: |
查看答案和解析>>
科目: 来源: 题型:阅读理解
查看答案和解析>>
科目: 来源: 题型:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| CuSO4 | 14.3 | 20.7 | 28.5 | 40.0 | 55.0 | 75.4 |
| Cu(NO3)2 | 81.8 | 124.8 | 163.1 | 181.8 | 207.8 | 247.3 |
| 实验步骤 | 预期现象 |
| 步骤1:除铁.将铜粉置于烧杯中, |
|
| 步骤2:溶解.将步骤1得到的铜粉置于烧杯中, |
|
| 步骤3:结晶.将步骤2所得溶液蒸发浓缩至液面有晶膜出现,冷却至室温,过滤得粗产品. | / |
查看答案和解析>>
科目: 来源: 题型:阅读理解
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3g/100gH2O | 8.08 | 12.6 | 18.3 | 24.8 |
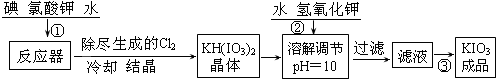
| 操 作 步 骤 | 实验现象 |
| 取1g纯净的NaCl,加3mL水配成溶液. | 溶液无变化 |
| 滴入5滴淀粉溶液和1mL 0.1mol/L KI溶液,振荡. | 溶液无变化 |
| 然后再滴入1滴1mol/L的H2SO4,振荡. | 溶液变蓝色 |
查看答案和解析>>
科目: 来源: 题型:
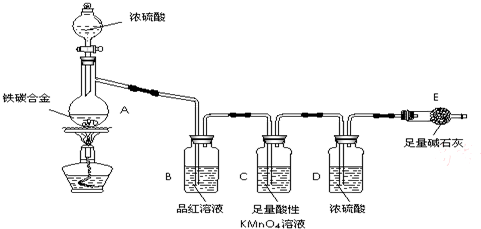
查看答案和解析>>
科目: 来源: 题型:阅读理解

查看答案和解析>>
科目: 来源: 题型:
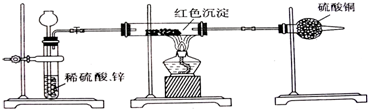
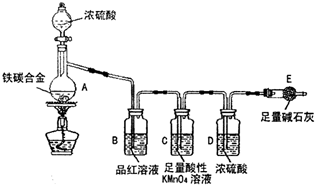 某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.
某化学兴趣小组为了测定某铁碳合金(看成铁和碳两种单质的混合物)中铁的质量分数,并探究浓硫酸的某些性质,设计了如图所示的装置(夹持仪器已省略)和方案进行实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com