
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、合成氨工业选择的反应条件不是室温,是500℃左右 | B、配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释 | C、实验室常用排饱和食盐水的方法收集氯气 | D、硫酸工业中,使用过量的空气以提高二氧化硫的利用率 |
查看答案和解析>>
科目: 来源: 题型:
| 化学方程式 | K(t1) | K(t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2=2HBr | 5.6×107 | 9.3×106 |
| I2+H2=2HI | 43 | 34 |
| A、在相同条件下随着卤素原子核电荷数的增加,平衡时X2的转化率逐渐降低 |
| B、t2>t1,HX的生成反应是吸热反应 |
| C、随着卤素原子核电荷数的增加HX的还原性逐渐减弱 |
| D、随着卤素原子核电荷数的增加HX的稳定性逐渐增强 |
查看答案和解析>>
科目: 来源: 题型:
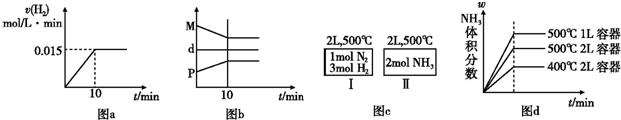
| A、若达到平衡时,测得体系放出9.24 kJ热量,则H2反应速率变化曲线如图a所示 | B、反应过程中,混合气体平均相对分子质量为M,混合气体密度为d,混合气体压强为P,三者关系如图b | C、如图c所示,容器Ⅰ和Ⅱ达到平衡时,NH3的体积分数为ω,则容器Ⅰ放出热量与容器Ⅱ吸收热量之和为92.4 kJ | D、若起始加入物料为1 mol N2,3 mol H2,在不同条件下达到平衡时,NH3的体积分数变化如图d所示 |
查看答案和解析>>
科目: 来源: 题型:
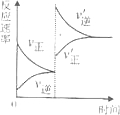 对达到平衡状态的可逆反应X+Y?Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则图象中关于X、Y、Z、W四种物质的聚集状态为( )
对达到平衡状态的可逆反应X+Y?Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则图象中关于X、Y、Z、W四种物质的聚集状态为( )| A、X、Y、Z、W皆非气体 | B、Z、W中有一种是气体,X、Y皆非气体 | C、Z、W均为气体,X、Y中有一种是气体 | D、X、Y均为气体,Z、W中有一种为气体 |
查看答案和解析>>
科目: 来源: 题型:
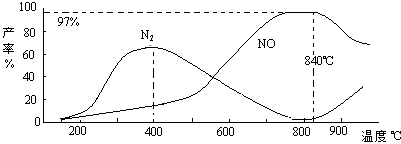
| A、840℃后升高温度,反应(ⅰ)的正反应速率减小,反应(ⅱ)的正反应速率增大 | B、升高温度,反应(ⅰ)和(ⅱ)的平衡常数均减小 | C、900℃后,NO产率下降的主要原因是反应(ⅰ)平衡逆向移动 | D、400℃-700℃,N2产率降低的主要原因是反应(ⅱ)平衡逆向移动 |
查看答案和解析>>
科目: 来源: 题型:
| A、对可逆反应,温度升高,反应速率增大,K值增大 | B、对可逆反应,温度不变,加催化剂,K值不变 | C、与化学反应本身和温度有关,并且会受到起始浓度的影响 | D、只与化学反应本身有关,与其他任何条件无关的一个不变的常数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com