
科目: 来源: 题型:
| A、先配制一定量的0.10mol?L-1的CH3COOH溶液,然后测溶液的pH,若pH大于1,则可证明醋酸为弱电解质 | B、先配制一定量0.01 mol?L-1和0.10 mol?L-1的CH3COOH溶液,分别用pH计测它们的pH,若两者的pH相差大于1个单位,则可证明醋酸是弱电解质 | C、先测0.10 mol?L-1 CH3COOH溶液的pH,然后将其加水稀释,再测pH,如果pH变大,则可证明醋酸是弱电解质 | D、配制一定量的CH3COONa溶液,测其pH,若常温下pH大于7,则可证明醋酸是弱电解质 |
查看答案和解析>>
科目: 来源: 题型:
| A、某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,则该溶液的pH 一定为14-a | B、某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度一定是:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c (H+) | C、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:c( R2-)+c(HR-)=c(Na+) | D、将0.2 mol/L的某一元酸HA溶液和0.1 mol/L NaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:2c( OH-)=2c( H+)+c(HA)-c(A-) |
查看答案和解析>>
科目: 来源: 题型:
| 下列说法正确的是( ) |
| A、标准状况下,3.36升HF溶于水配成l升溶液,溶液中F-浓度为0.15mol/L | ||||||||||
B、已知
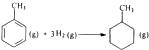 的△H为-384kJ?mol-1 的△H为-384kJ?mol-1 | ||||||||||
| C、常温下,pH=7的CH3COONa溶液中,c(CH3COO-)=c(Na+) | ||||||||||
| D、常温下,1升0.10 mol?L-1NH4C1溶液与2升0.05 mol?L-1NH4Cl溶液使中,所含NH+4的数目相等 |
查看答案和解析>>
科目: 来源: 题型:
一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的离子积.在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀.已知有关物质的颜色和溶度积如下:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com