
科目: 来源: 题型:
| 微粒 | H+ | OH- | CH3COO- | CH3OOH |
| 物质的量浓度 | 增大 | 减小 | 减小 | 增大 |
| A、氯化氢 | B、氢氧化钠 |
| C、蒸馏水 | D、醋酸 |
查看答案和解析>>
科目: 来源: 题型:
A、日本福岛核电站爆炸时释放的两种放射性核素
| ||||
| B、90℃时水的离子积KW=3.8×10-13,此时水的pH<7 | ||||
| C、依溶液导电能力的强弱,将电解质分为强、弱电解质 | ||||
| D、铝合金的大量使用,归功于人们能用焦炭等还原剂从氧化铝中获得铝 |
查看答案和解析>>
科目: 来源: 题型:
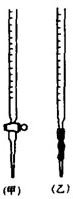 用中和滴定法测定某烧碱样品的纯度.有以下步骤:
用中和滴定法测定某烧碱样品的纯度.有以下步骤:| 测定序号 | 待测溶液的体积 /mL |
所耗盐酸标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com